논문 정보
- Title: Current landscape of plasma proteomics from technical innovations to biological insights and biomarker discovery
- Authors: Douglas Y. Kirsher, Shreya Chand, Aron Phong, Bich Nguyen, Balazs G. Szoke, Sara Ahadi
- Affiliation: Alkahest Inc., San Carlos, CA
- Journal: Communications Chemistry, Volume 8, Article 167 (2025)
- DOI: 10.1038/s42004-025-01665-1
연구 배경 및 동기
혈장(plasma)은 건강과 질병 상태를 반영하는 풍부한 생체분자의 원천이다. 특히 단백질은 생물학적 과정에서 핵심적인 역할을 수행하기 때문에, 바이오마커(biomarker)로서의 잠재력이 매우 높다. 최근 몇 년간 혈장 프로테옴(plasma proteome) 프로파일링 기술이 급속히 발전하면서, 질병 진단, 약물 타겟 발굴, 노화 연구 등 다양한 분야에서 활용이 확대되고 있다.
혈장 프로테오믹스에는 크게 두 가지 접근법이 존재한다:
- 친화성 기반(affinity-based) 플랫폼: 앱타머(aptamer)나 항체(antibody)와 같은 결합 프로브를 사용하여 단백질을 검출하는 방식으로, SomaScan, Olink Explore, NULISA 등이 대표적이다.
- 질량분석법(mass spectrometry, MS) 기반 플랫폼: 단백질을 분해하여 펩타이드(peptide) 수준에서 측정하는 bottom-up 방식으로, 번역 후 변형(PTM)이나 이소형(isoform)까지 식별할 수 있다.
그러나 이 다양한 플랫폼 간의 체계적인 성능 비교 연구는 여전히 부족한 실정이었다. Alkahest Inc.의 연구팀은 이 공백을 메우기 위해, 동일한 코호트(cohort)의 혈장 샘플을 8개 프로테오믹스 플랫폼으로 분석하여 각 플랫폼의 기술적 특성, 커버리지, 정밀도, 그리고 생물학적 통찰력을 직접 비교했다.
13,000개 이상의 단백질을 커버하는 8개 플랫폼을 동일 코호트에 적용한 가장 포괄적인 혈장 프로테오믹스 벤치마킹 연구
연구 설계 및 8개 플랫폼 개요
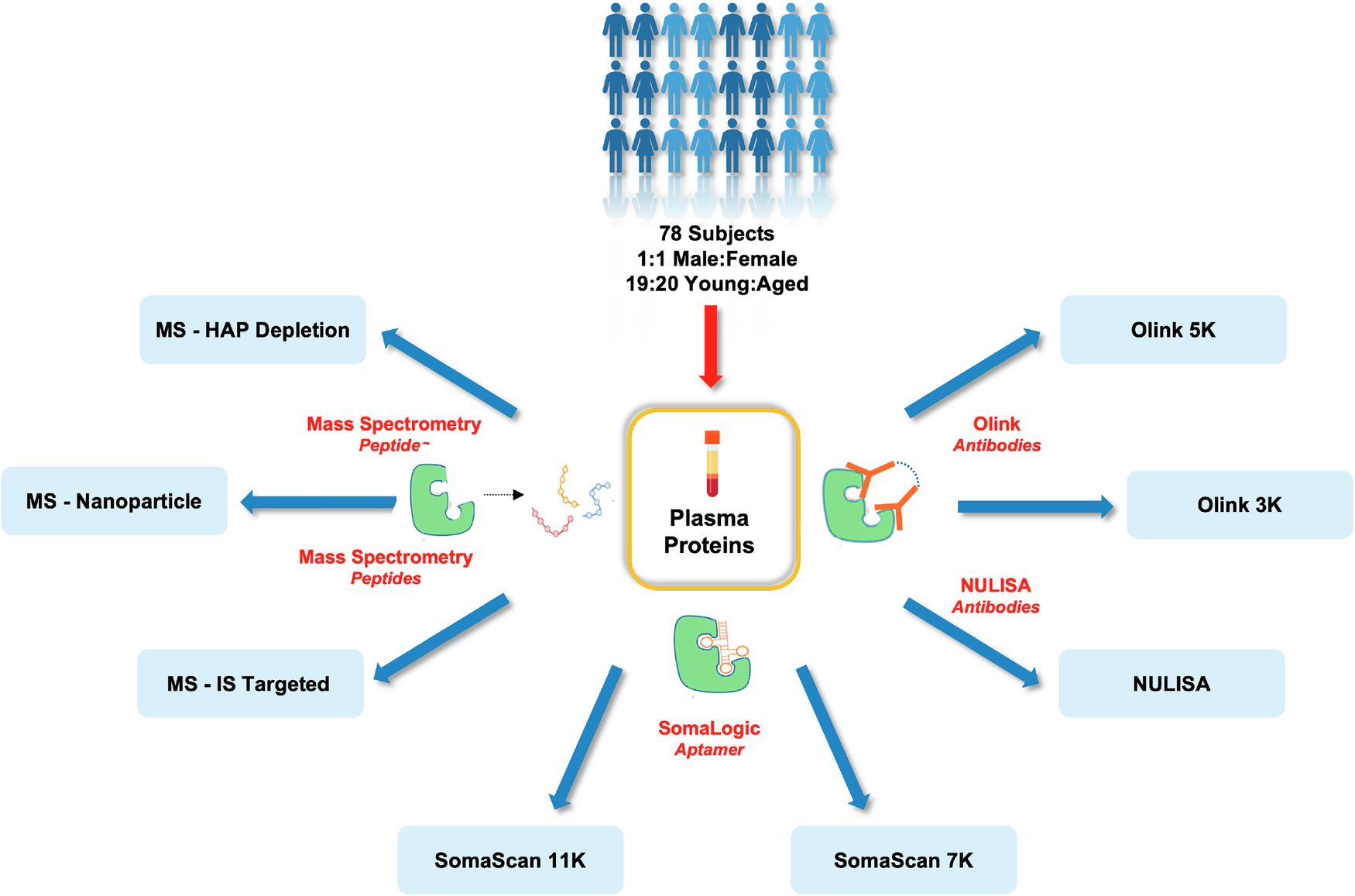 Figure 1: 연구 코호트 및 8개 프로테오믹스 플랫폼의 개요. 혈장분리반출법(plasmapheresis)으로 수집된 혈장 샘플을 8개 플랫폼으로 분석 (출처: Kirsher et al., Commun Chem 2025)
Figure 1: 연구 코호트 및 8개 프로테오믹스 플랫폼의 개요. 혈장분리반출법(plasmapheresis)으로 수집된 혈장 샘플을 8개 플랫폼으로 분석 (출처: Kirsher et al., Commun Chem 2025)
코호트
78명의 피험자(여성 39명, 남성 39명)를 두 그룹으로 나누어 구성했다:
| 그룹 | 인원 | 연령 범위 |
|---|---|---|
| 젊은 그룹(Young) | 38명 | 18–22세 |
| 고령 그룹(Aged) | 40명 | 55–65세 |
혈장 샘플은 혈장분리반출법(plasmapheresis)으로 수집하여 동일한 조건에서 8개 플랫폼에 적용했다.
8개 플랫폼
| 플랫폼 | 유형 | 기술 | 특징 |
|---|---|---|---|
| SomaScan 11K | 친화성 기반 | SOMAmer 앱타머 | 10,776개 인간 단백질 분석, 9,645개 고유 UniProt ID |
| SomaScan 7K | 친화성 기반 | SOMAmer 앱타머 | 6,401개 단백질 검출 |
| Olink Explore HT (5K) | 친화성 기반 | PEA (항체) | 5,400개 이상 분석 |
| Olink Explore 3072 (3K) | 친화성 기반 | PEA (항체) | 3,072개 분석 |
| MS-HAP Depletion | MS 기반 | Biognosys TrueDiscovery | 고농도 단백질 제거 후 DIA-MS |
| MS-Nanoparticle | MS 기반 | Seer Proteograph XT | 나노입자 기반 단백질 농축 |
| MS-IS Targeted | MS 기반 | SureQuant (PRM) | 내부 표준물질 기반 절대정량, “골드 스탠다드” |
| NULISA | 친화성 기반 | NULISAseq | 염증 패널 250 + CNS 질환 패널 120 |
단백질 커버리지 및 정밀도 비교
 Figure 2: 플랫폼 간 단백질 정량 및 검출 메트릭의 비교. UpSet 플롯을 통한 플랫폼별 단백질 식별 교집합 분석 (출처: Kirsher et al., Commun Chem 2025)
Figure 2: 플랫폼 간 단백질 정량 및 검출 메트릭의 비교. UpSet 플롯을 통한 플랫폼별 단백질 식별 교집합 분석 (출처: Kirsher et al., Commun Chem 2025)
커버리지
8개 플랫폼 전체에서 공유되는 단백질은 36개에 불과했다. NULISA를 제외한 7개 플랫폼에서는 259개 단백질이 공통으로 정량 가능했다. 이는 각 플랫폼이 프로테옴의 서로 다른 영역을 탐색하고 있음을 보여준다.
기술적 정밀도 (CV)
변동계수(coefficient of variation, CV)는 플랫폼의 재현성을 평가하는 핵심 지표다:
| 플랫폼 | 중위 CV (%) | 평가 |
|---|---|---|
| SomaScan 11K | 5.3 | 최고 정밀도 |
| SomaScan 7K | 5.8 | 우수 |
| MS-IS Targeted (SureQuant) | 8.3 | 우수 |
| Olink 3K | 11.4 | 양호 |
| MS-Nanoparticle (Proteograph XT) | 26.4 | 높은 변동 |
| Olink 5K | 26.8 | 높은 변동 |
| MS-HAP Depletion (TrueDiscovery) | 29.8 | 높은 변동 |
SomaScan 플랫폼이 모든 플랫폼 중 가장 낮은 기술적 변동계수를 보여, 재현성 측면에서 우위를 보였다.
데이터 완전성
| 플랫폼 | 데이터 완전성 (%) |
|---|---|
| SomaScan 11K | 96.2 |
| SomaScan 7K | 95.8 |
| Olink 5K | 35.9 |
SomaScan은 96% 이상의 데이터 완전성을 달성한 반면, Olink 5K는 35.9%에 그쳐 결측 데이터 처리에 주의가 필요하다.
FDA 바이오마커 커버리지
SomaScan 11K/7K는 FDA 승인 바이오마커의 88%/76%를 커버하여, 다른 모든 플랫폼을 상회했다. 이는 임상 바이오마커 발굴 연구에서 SomaScan의 강점을 보여준다.
플랫폼 간 교차 상관관계 분석
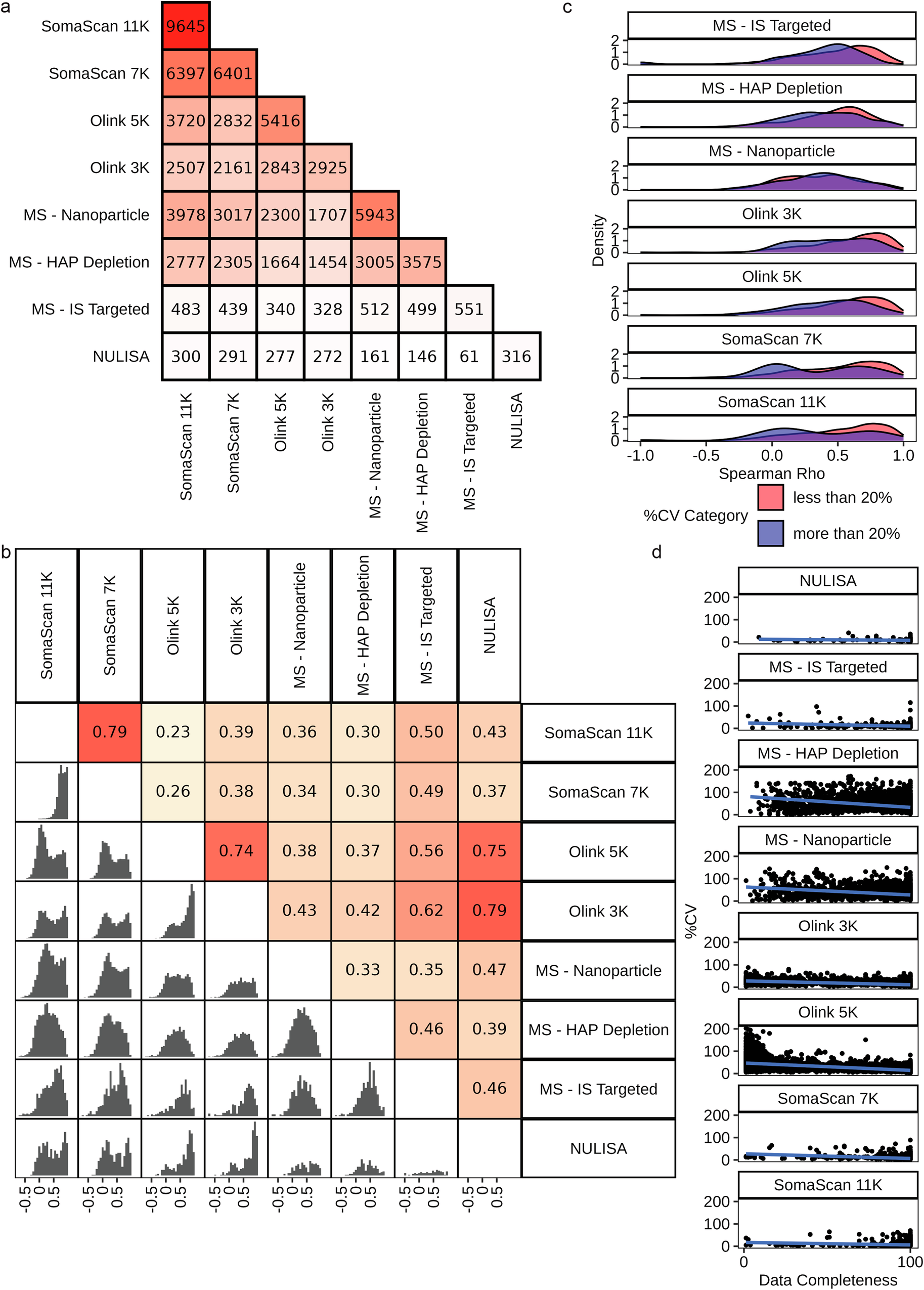 Figure 3: 플랫폼 간 공유 단백질의 비교 분석. (a) 플랫폼 쌍별 단백질 교집합 크기, (b) 단백질별 Spearman 상관계수 분포, (c) 259개 공유 단백질에 대한 밀도 플롯 (출처: Kirsher et al., Commun Chem 2025)
Figure 3: 플랫폼 간 공유 단백질의 비교 분석. (a) 플랫폼 쌍별 단백질 교집합 크기, (b) 단백질별 Spearman 상관계수 분포, (c) 259개 공유 단백질에 대한 밀도 플롯 (출처: Kirsher et al., Commun Chem 2025)
플랫폼 간 단백질 중복
가장 많은 단백질이 중복되는 조합은 SomaScan 11K와 MS-Nanoparticle 사이의 3,978개 단백질이었고, 그다음은 SomaScan 11K와 Olink 5K 사이의 3,720개였다.
플랫폼 내/간 Spearman 상관계수
| 플랫폼 쌍 | Spearman ρ | 의미 |
|---|---|---|
| SomaScan 11K ↔ 7K | 0.79 | 높은 내부 일관성 |
| Olink 5K ↔ 3K | 0.74 | 높은 내부 일관성 |
| NULISA ↔ Olink 3K | 0.79 | 기술적 유사성 + 상호 검증 |
| NULISA ↔ Olink 5K | 0.75 | 양호한 상관 |
동일 기술 계열의 플랫폼 간 상관관계가 높았으며, NULISA와 Olink 간에도 유의미한 상관이 관찰되었다. 이는 항체 기반 플랫폼 간의 기술적 유사성뿐만 아니라 상호 특이성 검증(mutual specificity validation)도 제공한다.
CV와 상관관계의 관계
259개 공유 단백질에 대한 분석에서, 기술적 CV가 20% 미만인 단백질은 다른 플랫폼과의 상관관계가 높은 경향을 보였다. 예를 들어:
- P11226 (MBL2): 모든 플랫폼 간 높은 상관 (Spearman 0.86–0.99)
- P07359 (GP1BA): 친화성 플랫폼 간에는 높은 상관(0.79–0.93)이지만, MS 플랫폼과는 낮은 상관(0.10–0.24)
이는 측정 정밀도가 플랫폼 간 일치도에 직접적인 영향을 미친다는 것을 의미한다.
APOE 이소형(Isoform) 비교
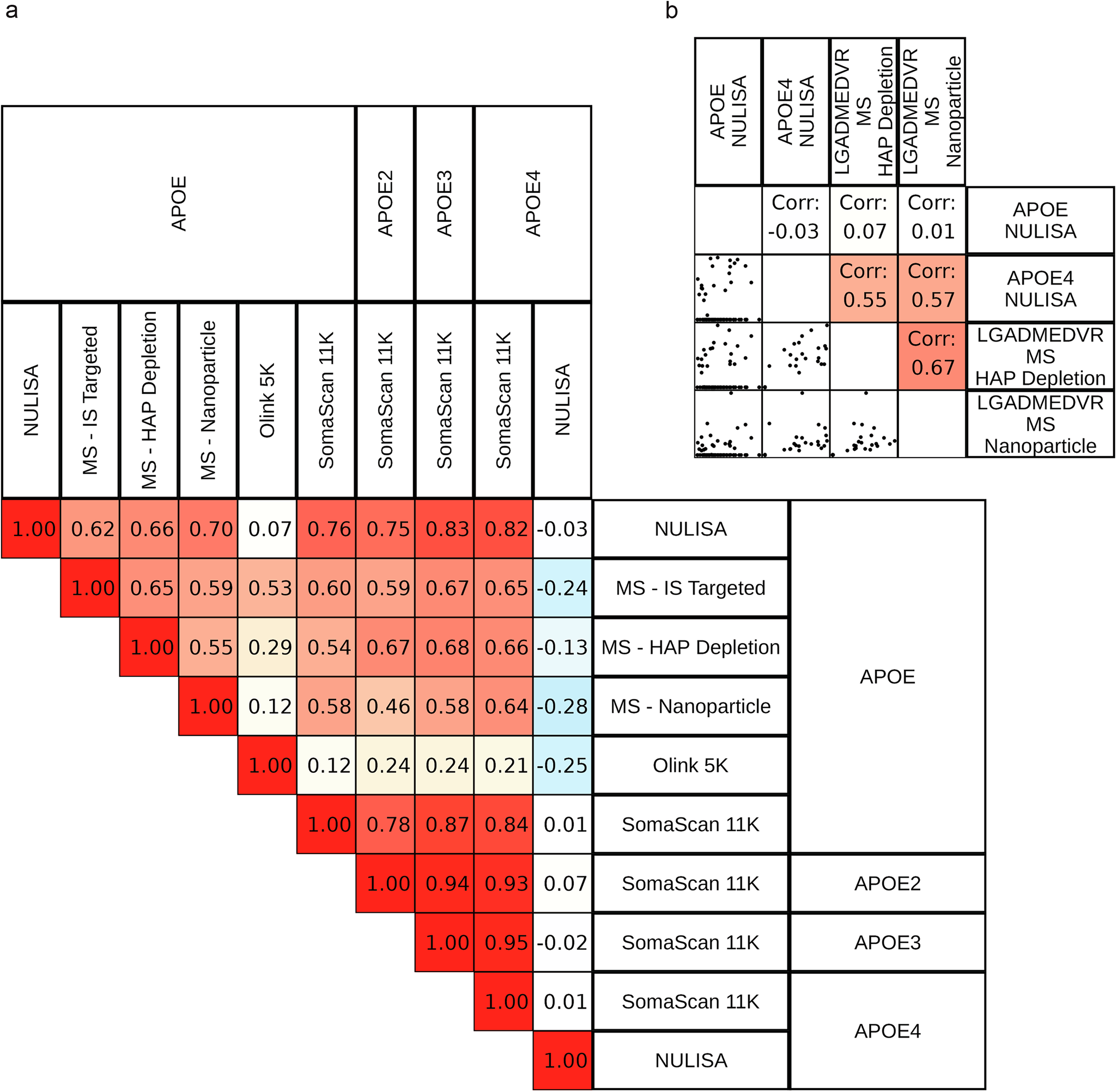 Figure 4: 다양한 프로테오믹스 플랫폼에서의 APOE 이소형 측정 비교. 플랫폼별 Spearman 상관관계와 산점도 (출처: Kirsher et al., Commun Chem 2025)
Figure 4: 다양한 프로테오믹스 플랫폼에서의 APOE 이소형 측정 비교. 플랫폼별 Spearman 상관관계와 산점도 (출처: Kirsher et al., Commun Chem 2025)
아포지단백질 E(APOE)는 알츠하이머병 등 신경퇴행성 질환 연구에서 핵심적인 바이오마커다. 특히 APOE4 대립유전자는 알츠하이머병의 주요 위험인자로, 이소형별(proteoform-specific) 측정이 중요하다.
플랫폼별 APOE 측정 능력
| 플랫폼 | 총 APOE | APOE2 | APOE3 | APOE4 |
|---|---|---|---|---|
| SomaScan 7K/11K | O | O | O | O |
| NULISA | O | X | X | O |
| Olink | O | X | X | X |
| MS 플랫폼 | O | X | X | 펩타이드 수준 |
대부분의 플랫폼은 총 APOE만 측정하지만, SomaScan 7K/11K는 3가지 이소형 모두에 대한 분석을 제공하고, NULISA는 APOE4를 특이적으로 측정한다.
주목할 만한 발견
- 총 APOE는 Olink 3K/5K를 제외한 플랫폼 간에 높은 상관관계를 보였다
- 예상 외로 NULISA의 APOE4 분석과 SomaScan의 APOE4 분석 간 상관관계가 없었다
- SomaScan의 4개 APOE 분석(총 APOE + 3개 이소형) 간 강한 상호 상관이 관찰되어, 이소형 선택성(isoform selectivity)이 부족할 가능성이 제기되었다
이는 현재 친화성 기반 플랫폼의 이소형 분별 능력에 한계가 있음을 시사하며, MS 기반 펩타이드 수준 분석이 이소형 연구에서 여전히 중요한 보완적 역할을 할 수 있음을 보여준다.
생물학적 예측 마커 및 분산 분석
 Figure 5: 플랫폼별 단백질 클래스, 예측 마커, 분산 분석. (a) PANTHER 단백질 클래스 비율, (b) 생물학적 예측인자별 마커 수, (c) 생물학적 요인에 의한 분산 설명 비율, (d) 미설명 분산 50% 이상 단백질의 PANTHER 클래스 (출처: Kirsher et al., Commun Chem 2025)
Figure 5: 플랫폼별 단백질 클래스, 예측 마커, 분산 분석. (a) PANTHER 단백질 클래스 비율, (b) 생물학적 예측인자별 마커 수, (c) 생물학적 요인에 의한 분산 설명 비율, (d) 미설명 분산 50% 이상 단백질의 PANTHER 클래스 (출처: Kirsher et al., Commun Chem 2025)
생물학적 예측인자별 마커 발견
연구팀은 나이(age), 성별(sex), BMI, 흡연 상태(smoking), 인종(race) 등 임상 정보와 프로테오믹 데이터를 결합하여, 각 플랫폼이 생물학적으로 유의미한 단백질 마커를 얼마나 많이 탐지하는지 평가했다.
모든 플랫폼이 일부 연관성을 식별했지만, SomaScan 플랫폼이 임상 측정별로 수백~수천 개의 단백질을 탐지하여 다른 플랫폼을 크게 상회했다. 친화성 기반 플랫폼이 전반적으로 가장 많은 고유 및 공유 노화 마커를 기여한 반면, MS 발견 플랫폼과 표적 MS 플랫폼은 적은 수의 유의미한 마커를 식별했지만, 친화성 플랫폼이 커버하지 못하는 가치 있는 단백질을 추가로 제공했다.
분산 설명 비율
| 플랫폼 | 분산 설명 비율 (%) |
|---|---|
| NULISA | 22.9 |
| MS-IS Targeted | ~22 |
| Olink 3K | ~21 |
| MS-Nanoparticle | ~20 |
| SomaScan 7K | ~20 |
| SomaScan 11K | 19.9 |
| Olink 5K | ~14.5 |
| MS-HAP Depletion | 13.8 |
NULISA, MS-IS Targeted, Olink 3K, MS-Nanoparticle, SomaScan 7K/11K는 비교적 유사한 수준의 분산(19.9–22.9%)을 설명한 반면, Olink 5K와 MS-HAP Depletion은 상대적으로 낮은 설명력(13.8–14.5%)을 보였다.
플랫폼 업그레이드의 효과
- SomaScan 11K는 SomaScan 7K에서 발견하지 못한 118개의 추가 노화 마커를 식별
- Olink 5K는 이전 버전(3K)에서 검출되지 않았던 68개의 고유 노화 단백질을 탐지
이는 플랫폼 업그레이드가 단순히 커버리지 확장뿐만 아니라, 새로운 생물학적 통찰을 제공할 수 있음을 보여준다.
PANTHER 단백질 클래스 분석
모든 플랫폼에서 30% 이상의 비율로 공통적으로 나타난 단백질 클래스는:
- 아포지단백질(apolipoprotein)
- 보체(complement component)
- 프로테아제 억제제(protease inhibitor)
- 표면활성제 단백질(surfactant protein)
SomaScan 11K/7K가 PANTHER 분류 체계에서 가장 다양한 단백질 클래스를 가장 깊은 수준으로 커버했다.
UK Biobank 데이터와의 교차 검증
제한된 코호트 크기에도 불구하고, 각 플랫폼이 식별한 마커와 UK Biobank 데이터셋의 마커 사이에 유의미한 중복이 관찰되어, 발견된 노화 관련 마커의 생물학적 타당성(biological relevance)이 뒷받침되었다.
의의 및 한계
의의
- 가장 포괄적인 벤치마킹: 8개 플랫폼을 동일 코호트에 적용하여 직접 비교한 최초의 대규모 연구로, 프로테오믹스 연구자들에게 플랫폼 선택의 근거를 제공
- 상호보완성 입증: 단일 플랫폼만으로는 프로테옴의 전체 그림을 파악할 수 없으며, 다중 플랫폼 전략(multi-platform strategy)이 필요하다는 것을 정량적으로 증명
- 이소형 분석의 한계 규명: APOE 이소형 분석에서 친화성 기반 플랫폼의 선택성 한계를 발견하여, 향후 분석 개선의 방향을 제시
- 실용적 가이드라인: 연구 목적(커버리지 vs. 정밀도 vs. 특이성)에 따른 플랫폼 선택 기준을 제공
한계
- 코호트 크기: 78명으로 비교적 소규모이며, 나이 범위도 18–22세와 55–65세로 제한되어 있어 중간 연령대의 변화를 포착하지 못함
- 단일 기관 연구: Alkahest Inc. 단독 수행으로, 독립적 재현 연구가 필요
- 플랫폼 간 직접 정량 비교의 어려움: 각 플랫폼의 측정 단위와 정규화 방법이 다르기 때문에, 절대값 수준의 비교에는 한계 존재
- NULISA의 제한된 커버리지: NULISA는 370개 분석에 그쳐 다른 플랫폼과의 비교 범위가 제한적
개인적 소감
이 논문은 혈장 프로테오믹스 분야에서 오랫동안 필요했던 체계적인 플랫폼 벤치마킹을 수행한 중요한 연구다. 특히 인상적인 부분은:
-
“최고의 플랫폼은 없다”는 명확한 메시지: SomaScan은 커버리지와 정밀도에서, Olink는 타겟 특이성과 유전적 검증에서, MS는 비편향적 검출과 이소형 분석에서, NULISA는 민감도에서 각각 강점을 보인다. 이는 연구 목적에 따른 맞춤형 플랫폼 선택의 중요성을 강조한다.
-
노화 연구에의 함의: 젊은 그룹(18–22세)과 고령 그룹(55–65세)의 비교에서 플랫폼별로 서로 다른 노화 마커를 발견한 점은, 다중 오믹스(multi-omics) 접근이 노화의 복잡한 분자 기전을 이해하는 데 필수적이라는 것을 다시 한번 확인해준다.
-
APOE 이소형 분석의 시사점: 알츠하이머병 연구에서 APOE4의 정확한 정량이 얼마나 어려운지를 보여준 부분이 특히 흥미롭다. 친화성 기반 플랫폼의 이소형 선택성 한계는 향후 프로브 설계 개선의 중요한 과제가 될 것이다.
노화 연구 관점에서, 이 논문이 제시한 플랫폼별 성능 데이터는 혈장 프로테오믹 에이징 클락(proteomic aging clock) 개발에서 어떤 플랫폼을 선택할지에 대한 실질적인 가이드라인이 된다. 커버리지가 중요한 탐색 단계에서는 SomaScan 11K가, 특정 마커의 검증 단계에서는 MS-IS Targeted(SureQuant)가, 그리고 민감한 저농도 바이오마커 검출에는 NULISA가 최적의 선택이 될 수 있을 것이다.
References
- Kirsher, D.Y., Chand, S., Phong, A., Nguyen, B., Szoke, B.G. & Ahadi, S. Current landscape of plasma proteomics from technical innovations to biological insights and biomarker discovery. Commun Chem 8, 167 (2025). https://doi.org/10.1038/s42004-025-01665-1
-
PubMed PMC Full Text bioRxiv Preprint
💬 댓글