Li S, Hamaya R, Zhu H, Chen BH, Pereira AC, Ivey KL, Rist PM, Manson JE, Dong Y & Sesso HD. Effects of daily multivitamin–multimineral and cocoa extract supplementation on epigenetic aging clocks in the COSMOS randomized clinical trial. Nature Medicine (2026). https://doi.org/10.1038/s41591-026-04239-3
배경: 왜 종합비타민과 에피제네틱 시계를 함께 봐야 할까?
전 세계 성인 질병 부담의 절반가량이 노화 관련 질환에서 비롯된다. 게로사이언스 가설(geroscience hypothesis)은 노화 속도 자체를 늦추는 개입이 암, 심혈관 질환, 인지 저하 등 다양한 노인성 질환을 동시에 예방·지연할 수 있다고 제안한다.
이를 측정하는 핵심 도구 중 하나가 에피제네틱 클락(epigenetic clock)이다. 혈액 내 DNA 메틸화(DNAm) 패턴을 분석해 ‘생물학적 나이(biological age)’를 추정하는 알고리즘으로, 단순한 역연령(chronological age)보다 사망률·이환율 예측력이 높다.
한편 종합비타민·미네랄(multivitamin-multimineral, MVM)은 미국 내 가장 흔하게 복용되는 영양 보충제다. 이전 COSMOS(COcoa Supplement and Multivitamin Outcomes Study) 본시험에서 MVM은 인지 저하 억제, 폐암 위험 38% 감소 등 여러 노화 관련 이점이 보고되었다. 그러나 MVM이 DNA 메틸화 수준에서 생물학적 노화 자체를 늦추는지는 불분명했다.
이 연구는 바로 그 물음에 답하기 위한 COSMOS 전향적 무작위대조시험(RCT) 부속 연구다.
연구 설계
COSMOS 시험 개요
COSMOS는 2016–2018년 미국에서 65세 이상 여성·60세 이상 남성 21,442명을 대상으로 진행된 대규모 이중맹검 무작위대조시험이다. 2×2 요인 설계로 네 군에 배정했다:
- 코코아 추출물 활성 + MVM 활성
- 코코아 추출물 활성 + MVM 위약
- 코코아 추출물 위약 + MVM 활성
- 코코아 추출물 위약 + MVM 위약
- MVM: Centrum Silver (Pfizer/Haleon)
- 코코아 추출물: 하루 코코아 플라바놀(flavanol) 500 mg ((-)-에피카테킨 80 mg 포함)
이번 부속 연구 대상
COSMOS Blood 서브코호트(6,867명) 중 베이스라인·1년·2년 혈액을 모두 제공한 1,829명에서, DNAm 분석을 위해 998명을 무작위 선정했다(유색인종 과잉 표집, 성별 균형 유지). 최종 분석에는 958명, 2,815개 샘플이 포함되었다.
 Fig. 1. 연구 참가자 흐름도. 21,442명 중 최종 958명(MVM 위약 482명 / 활성 476명, 코코아 위약 433명 / 활성 525명)이 분석에 포함됐다.
Fig. 1. 연구 참가자 흐름도. 21,442명 중 최종 958명(MVM 위약 482명 / 활성 476명, 코코아 위약 433명 / 활성 525명)이 분석에 포함됐다.
포함 기준: 베이스라인에서 주요 만성질환 없음 + 혈액 채취 후 2년간 심혈관 사건(심근경색·뇌졸중·관상동맥 재개통술) 및 침습성 암 미발생자.
주요 베이스라인 특성:
| 항목 | 값 |
|---|---|
| 평균 연령 | 70.2 ± 5.6세 |
| 여성 비율 | 50.3% |
| 백인 비율 | 89.1% |
| 고혈압 | 53.6% |
| 당뇨 | 12.9% |
| 2년 순응률(MVM) | 91.9% |
| 2년 순응률(코코아) | 95.1% |
에피제네틱 클락: 어떤 지표를 사용했나?
이 연구는 세 세대에 걸친 5종의 DNAm 기반 생물학적 노화 지표를 분석했다.
1세대 클락 — 역연령 예측
| 클락 | 특징 |
|---|---|
| PCHorvath | 다조직(multi-tissue) 클락, 역연령과 높은 상관 (r = 0.81) |
| PCHannum | 혈액 기반 클락 (r = 0.77) |
1세대 클락은 역연령과 높은 상관을 보이나, 사망률 예측력은 상대적으로 낮고 개입에 덜 민감하다.
2세대 클락 — 사망 위험 반영
| 클락 | 특징 |
|---|---|
| PCPhenoAge | 9가지 혈액 임상 마커를 기반으로 ‘표현형 나이’ 예측 |
| PCGrimAge | 텔로미어 길이, 사이토카인 등 9종 DNAm 대리지표를 활용해 전사망률 예측 |
2세대 클락은 주요 이환율·사망률과 강하게 연관되며, 개입 연구의 반응성이 높은 것으로 알려져 있다.
3세대 클락 — 노화 속도 측정
| 클락 | 특징 |
|---|---|
| DunedinPACE | 19개 생리 지표의 종단 변화율을 기반으로 노화 ‘속도’ 측정. 1 = 기준, >1이면 빠른 노화 |
PC 버전 사용의 의의: 1·2세대 클락은 반복 측정 시 기술적 노이즈가 있어, Higgins-Chen et al. (2022)이 개발한 주성분(PC) 재훈련 버전을 적용해 측정 신뢰도를 높였다 (ICC: PCHorvath 0.937, PCGrimAge 0.919).
주요 결과
MVM의 효과
2년간 MVM 복용은 2세대 에피제네틱 클락의 증가 속도를 유의하게 늦췄다.
| 클락 | 연간 군간 차이 | 95% CI | P값 |
|---|---|---|---|
| PCPhenoAge | −0.214년 | −0.410 ~ −0.019 | 0.032 |
| PCGrimAge | −0.113년 | −0.205 ~ −0.020 | 0.017 |
| PCHorvath | −0.019년 | −0.127 ~ 0.089 | 0.731 |
| PCHannum | −0.058년 | −0.195 ~ 0.079 | 0.405 |
| DunedinPACE | −0.003 | −0.007 ~ 0.001 | 0.191 |
2년 시점 절대 차이: PCPhenoAge −0.443년 (P=0.033), PCGrimAge −0.209년 (P=0.030).
효과 크기(Cohen’s d)는 −0.033 ~ −0.038로 소규모(small effect)이지만 통계적으로는 유의했다.
주목할 점은 DunedinPACE다. 위약군에서는 유의하게 증가했지만 MVM군에서는 안정적으로 유지됐다. 비록 군간 차이가 통계적 유의성에 도달하지 못했지만, 1년→2년으로 갈수록 효과 크기가 커지는 추세가 관찰됐다.
 Fig. 2. MVM군(검정)과 위약군(회색)의 베이스라인 대비 변화. 왼쪽 박스플롯은 관측값, 오른쪽 선그래프는 혼합 모형 추정치와 95% CI. PCPhenoAge(c)와 PCGrimAge(d)에서 MVM군의 유의한 증가 억제가 확인된다.
Fig. 2. MVM군(검정)과 위약군(회색)의 베이스라인 대비 변화. 왼쪽 박스플롯은 관측값, 오른쪽 선그래프는 혼합 모형 추정치와 95% CI. PCPhenoAge(c)와 PCGrimAge(d)에서 MVM군의 유의한 증가 억제가 확인된다.
코코아 추출물의 효과
코코아 추출물은 5개 클락 모두에서 유의한 효과를 보이지 않았다. 오히려 PCPhenoAge에서 약간의 증가 경향(+0.202년/년, P=0.044)이 관찰됐는데, 이는 코코아군의 베이스라인 PCPhenoAge AgeDev가 상대적으로 낮았던 데 따른 평균으로의 회귀(regression to the mean) 효과로 해석된다.
 Fig. 3. 코코아 추출물군(검정)과 위약군(회색)의 에피제네틱 클락 변화. 5개 클락 모두에서 군간 유의한 차이가 없었다.
Fig. 3. 코코아 추출물군(검정)과 위약군(회색)의 에피제네틱 클락 변화. 5개 클락 모두에서 군간 유의한 차이가 없었다.
가속 노화 그룹에서 더 강한 MVM 효과
가장 흥미로운 발견 중 하나는 베이스라인에서 생물학적 노화가 가속된 참가자에서 MVM의 효과가 더 강하다는 것이다.
| 그룹 | PCGrimAge 연간 군간 차이 | 95% CI |
|---|---|---|
| 가속 노화 (AgeDev > 0) | −0.236년 | −0.380 ~ −0.091 |
| 정상/감속 노화 (AgeDev ≤ 0) | −0.013년 | −0.130 ~ 0.104 |
| 상호작용 P값 | 0.018 |
PCPhenoAge에서도 유사: 가속 노화군 −0.394년 vs 정상군 −0.075년 (P for interaction=0.106).
DunedinPACE에서도 같은 방향 — 빠른 노화군(DunedinPACE>1)에서 −0.007, 느린 노화군에서 0 (P for interaction=0.122).
이 패턴은 영양 결핍이 생물학적 노화 가속의 한 원인이며, MVM이 영양 불균형을 교정함으로써 노화를 늦춘다는 해석을 뒷받침한다.
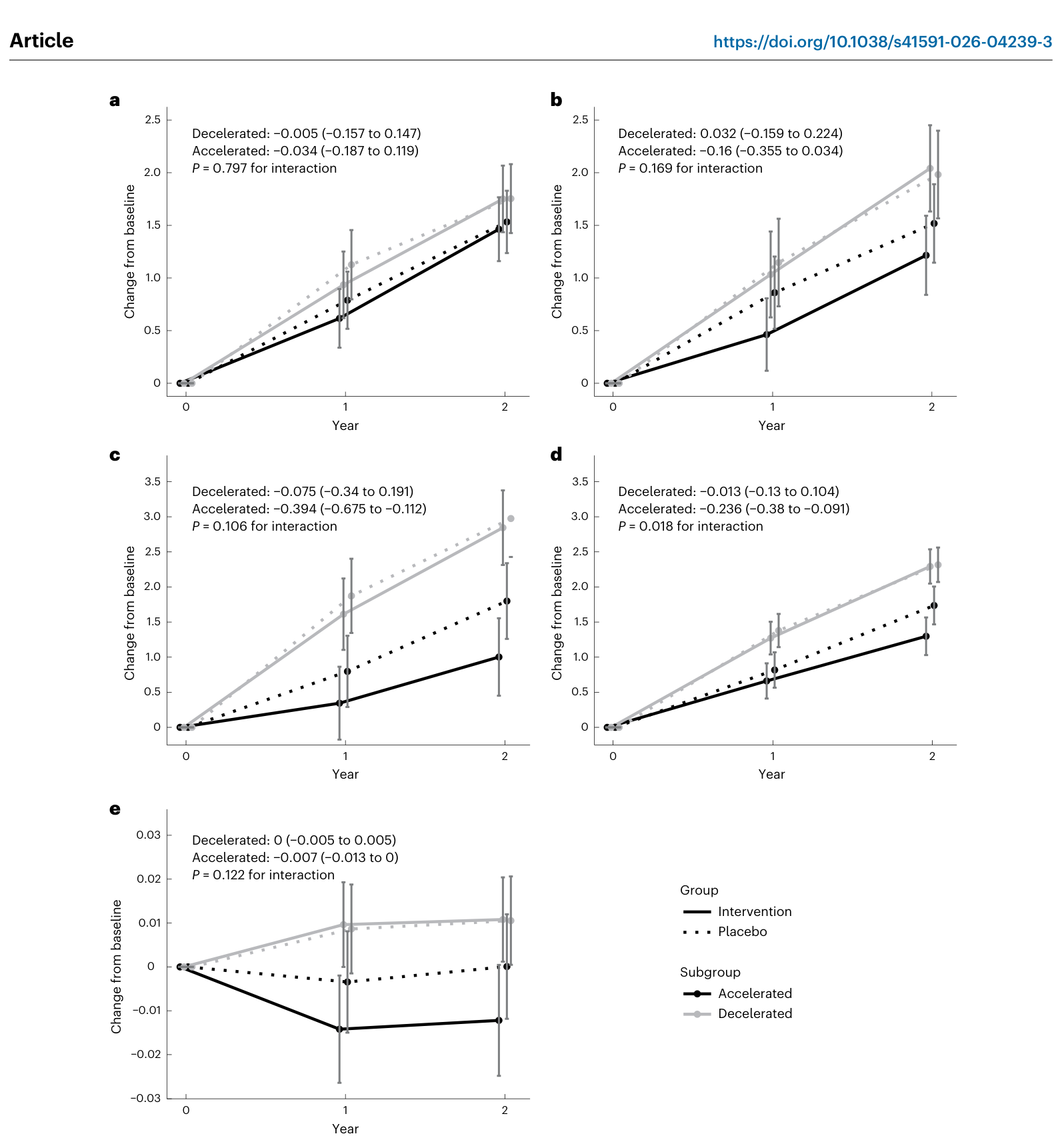 Fig. 4. 베이스라인 에피제네틱 노화 가속(검정) vs. 감속(회색) 그룹별 MVM(실선) vs. 위약(점선) 효과. PCGrimAge(d)에서 가속 노화군의 MVM 효과가 유의하게 더 컸다 (상호작용 P=0.018).
Fig. 4. 베이스라인 에피제네틱 노화 가속(검정) vs. 감속(회색) 그룹별 MVM(실선) vs. 위약(점선) 효과. PCGrimAge(d)에서 가속 노화군의 MVM 효과가 유의하게 더 컸다 (상호작용 P=0.018).
GrimAge 구성 성분 분석
MVM이 PCGrimAge를 낮추는 메커니즘을 탐색하기 위해 GrimAge 구성 DNAm 지표를 개별 분석했다:
| DNAm 지표 | MVM 효과 | P값 | 생물학적 의미 |
|---|---|---|---|
| 텔로미어 길이 (DNAmTL) | +0.022 | 0.027 | 세포 노화 억제 |
| 베타-2 마이크로글로불린 (B2M) | −0.028 | 0.002 | 면역·염증 조절 |
| 시스타틴 C (CystatinC) | −0.027 | 0.001 | 신장 기능 |
| GDF-15 | −0.029 | 0.001 | 미토콘드리아 기능 |
MVM이 세포 노화(텔로미어), 면역 노화(B2M), 신장 기능(Cystatin C), 미토콘드리아 기능(GDF-15) 등 다차원적 노화 경로에 광범위하게 작용함을 시사한다.
매개 분석: 인지 기능과 염증 지표
COSMOS-Mind 및 COSMOS Inflammaging 부속 연구 참가자와 중복된 그룹에서 탐색적 매개 분석을 수행했다:
- 인지 기능: PCPhenoAge·PCGrimAge 변화가 에피소딕 기억 개선의 4.1–5.2%를 매개 (통계적 유의성 미달)
- IL-6, IL-10: PCGrimAge·PCPhenoAge 변화가 MVM 관련 감소의 25.1–70.0% 설명 (통계적 유의성 미달)
샘플 규모 한계로 유의성에 도달하지 못했지만, 에피제네틱 노화 지연이 임상적 이점의 일부 경로일 가능성을 시사한다.
논의: 이 결과를 어떻게 해석할 것인가?
임상적 의의
연간 0.113–0.214년의 생물학적 노화 감속은 2년 기준 2.7–5.1개월의 노화 지연에 해당한다. 이전 역학 연구들의 연관성을 기반으로 환산하면, 이는 10년간 암 발생 위험 3–7% 감소에 상응하는 수준으로, COSMOS 본시험의 임상 결과(폐암 38% 감소)와 개념적으로 일관된다.
왜 1세대 클락은 반응이 없었나?
1세대 클락(Horvath, Hannum)은 역연령 예측에 최적화되어 있어 개입에 덜 민감하다. 실제로 CALERIE(열량 제한) 시험, DO-HEALTH(오메가-3) 시험 등 다른 노화 개입 연구들도 2세대 클락에서 효과가 더 뚜렷하게 나타났다.
코코아 추출물은 왜 효과가 없었나?
- 연구 참가자가 주요 만성질환 없는 건강한 노인으로, 코코아 플라바놀이 표적으로 하는 심혈관·염증 경로의 이상이 적었을 것
- 에피제네틱 클락이 코코아 효과의 주요 경로인 심혈관 관련 CpG 부위를 충분히 포함하지 않을 가능성 (CVD 관련 CpG의 다수가 기존 클락에 미포함)
CALERIE 시험과의 비교
| CALERIE (열량 제한) | COSMOS (MVM) | |
|---|---|---|
| 평균 연령 | 38세 | 70세 |
| 기간 | 2년 | 2년 |
| DunedinPACE | 2–3% 감소 (Cohen’s d=0.2–0.3) | 비유의 (−0.3%) |
| GrimAge/PhenoAge | 비유의 | 유의 (Cohen’s d=0.03) |
노인 참가자에서 이미 수십 년간 축적된 분자 변화를 2년 만에 역전하기 어렵다는 점, DunedinPACE가 26–45세 기반으로 개발되어 70세 고령자에서의 반응성에 한계가 있을 수 있다는 점을 고려해야 한다.
한계점
- 일반화 가능성: 참가자의 89%가 비히스패닉계 백인, 이미 건강한 고령자에 국한
- 다중비교 미보정: 클락들 간 높은 상관관계로 인해 Bonferroni 보정 미적용 (위양성 가능성)
- 2년이라는 단기 추적: 더 긴 기간에서 효과가 더 커질 가능성
- 매개 분석의 통계력 부족: 임상 결과와의 연결을 확인하기에 샘플 규모가 작음
- 에피제네틱 클락의 포괄성: 모든 생물학적 노화 변화가 현 클락에 포착되지 않음
개인 소감
이 논문이 흥미로운 이유는 단순히 “종합비타민이 몸에 좋다”는 메시지를 넘어, 에피제네틱 클락을 노화 개입의 중간 생물지표(surrogate biomarker)로 활용하는 방법론적 가능성을 대규모 RCT에서 탐색했다는 데 있다.
특히 가속 노화 그룹에서의 차별적 효과는 임상적으로 중요한 함의를 가진다. “이미 노화가 빠른 사람일수록 MVM이 더 효과적”이라는 발견은 개인화된 노화 개입(precision geroscience)의 가능성을 열어준다.
다만 Cohen’s d = 0.03이라는 효과 크기는 통계적으로 유의하지만 임상적으로 매우 작다는 점을 직시해야 한다. 에피제네틱 클락의 변화가 실제 임상 결과(수명 연장, 질환 예방)로 이어지는지는 더 긴 추적 기간과 더 큰 표본이 필요하다.
결론적으로, 매일 종합비타민 한 알이 생물학적 노화를 극적으로 되돌리는 것은 아니지만, 저비용·고접근성 개입으로서 특히 영양 불균형이 있는 고령자에게 의미 있는 노화 지연 효과를 줄 수 있다는 가능성을 제시한 의미 있는 연구다.
References
- Li S et al. Effects of daily multivitamin–multimineral and cocoa extract supplementation on epigenetic aging clocks in the COSMOS randomized clinical trial. Nature Medicine (2026). https://doi.org/10.1038/s41591-026-04239-3
- Belsky DW et al. DunedinPACE, a DNA methylation biomarker of the pace of aging. eLife 11, e73420 (2022).
- Lu AT et al. DNA methylation GrimAge strongly predicts lifespan and healthspan. Aging (Albany NY) 11, 303–327 (2019).
- Higgins-Chen AT et al. A computational solution for bolstering reliability of epigenetic clocks: implications for clinical trials and longitudinal tracking. Nature Aging 2, 644–661 (2022).
- Waziry R et al. Effect of long-term caloric restriction on DNA methylation measures of biological aging in healthy adults from the CALERIE trial. Nature Aging 3, 248–257 (2023).
- Bischof-Ferrari HA et al. Individual and additive effects of vitamin D, omega-3 and exercise on DNA methylation clocks of biological aging in older adults from the DO-HEALTH trial. Nature Aging 5, 376–385 (2025).
💬 댓글