Heritability of intrinsic human life span is about 50% when confounding factors are addressed Ben Shenhar, Glen Pridham, Thaís Lopes De Oliveira, Naveh Raz, Yifan Yang, Joris Deelen, Sara Hägg, Uri Alon Science 391, 6784 (2026). DOI: 10.1126/science.adz1187
연구 배경
인간 수명의 유전율(heritability)은 노화 연구의 핵심 질문 중 하나다. 유전율이 높다면, 장수 관련 유전자를 찾아 노화 메커니즘을 이해하고 의학·공중보건에 적용할 수 있는 가능성이 열린다.
그러나 지금까지의 추정치는 실망스러웠다. 기존 쌍둥이 연구들은 수명의 유전율을 20~25% 수준으로 보고했고, 최근 대규모 족보(pedigree) 데이터를 분석한 연구들은 이를 6~16%까지 낮게 추정했다. 이는 마우스(38~55%)나 다른 인간 생리적 형질의 평균 유전율(약 49%)과 비교해 현저히 낮은 수치다.
이러한 불일치가 연구자들의 의문을 자극했다. Shenhar et al.은 기존 추정치를 낮추는 교란 요인이 존재한다고 주장하며, 그 핵심으로 외인성 사망률(extrinsic mortality)을 지목했다.
핵심 개념: 내인성 사망 vs 외인성 사망
| 구분 | 정의 | 예시 |
|---|---|---|
| 외인성 사망률 (extrinsic mortality) | 신체 외부 요인에 의한 사망 | 사고, 살인, 감염병, 환경 위해 |
| 내인성 사망률 (intrinsic mortality) | 신체 내부 과정에 의한 사망 | 유전적 돌연변이, 노화 관련 질병, 생리 기능 저하 |
대부분의 쌍둥이 코호트는 18~19세기에 태어난 사람들로 구성되어 있어, 현재보다 약 10배 높은 외인성 사망률을 경험했다. 또한 이 역사적 코호트들은 사망 원인 데이터가 부재하여 두 사망 유형을 구분하기 어려웠다.
방법론
수학적 모델링
연구진은 전체 사망률을 다음과 같이 분해했다:
\[m(t) = m_{ex} + f(t, \vec{\theta})\]- $m_{ex}$: 연령 독립적인 외인성 사망률 상수
- $f(t, \vec{\theta})$: 연령 의존적 내인성 사망률 (파라미터 $\vec{\theta}$는 유전적으로 변이 가능)
두 가지 수리 모델을 사용했다:
- MGG 모델 (Makeham-Gamma-Gompertz): 사망 데이터에 대한 유연한 경험적 피팅 모델
- SR 모델 (Saturating-Removal): 손상 축적과 포화되는 제거 과정 간의 상호작용에서 노화가 발생하는 생물학적 기계론적 모델
분석 코호트
| 코호트 | 출생 연도 | 쌍둥이 쌍 수 | 외인성 사망률 ($m_{ex}$) |
|---|---|---|---|
| 덴마크 쌍둥이 | 1870–1900 | MZ 1,033쌍 / DZ 1,839쌍 | 4.0 × 10⁻³ year⁻¹ |
| 스웨덴 쌍둥이 | 1886–1925 | MZ 3,477쌍 / DZ 6,403쌍 | 2.78 × 10⁻³ year⁻¹ |
| SATSA (스웨덴) | 1900–1935 | MZ 196쌍 / DZ 325쌍 + 별거 쌍둥이 | 1.53 × 10⁻³ year⁻¹ |
| 미국 백세인의 형제자매 | 1873–1910 | 2,092명 | ~3.5 × 10⁻³ year⁻¹ |
유전율은 Falconer의 공식 $h^2 = 2(r_{MZ} - r_{DZ})$를 사용해 산출했다.
주요 결과
1. 외인성 사망률이 유전적 상관관계를 은폐한다
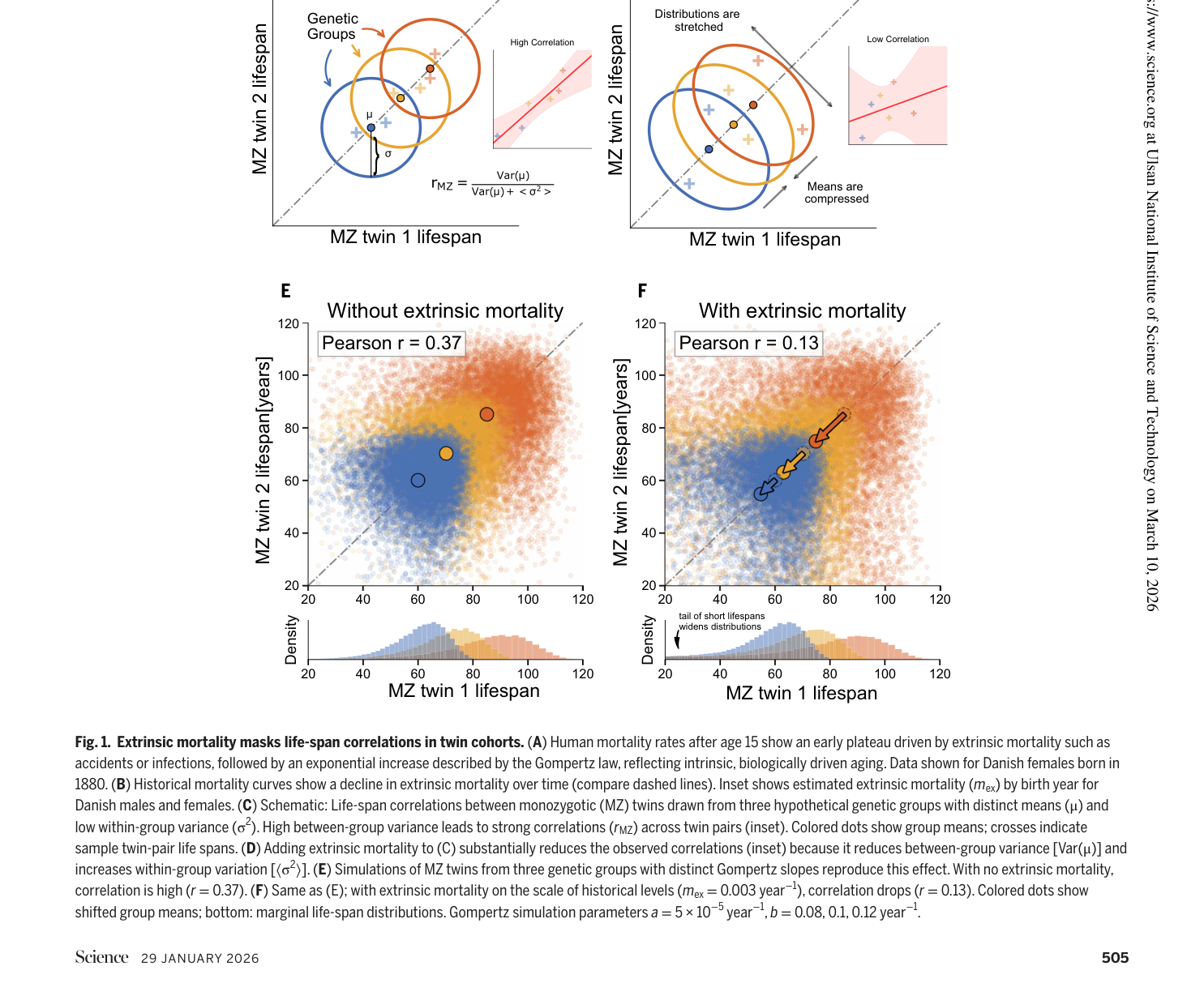 Fig. 1. 외인성 사망률이 쌍둥이 코호트의 수명 상관관계를 은폐한다. (A) 1880년 출생 덴마크 여성의 연령별 사망률: 20~40세 구간에 외인성 사망률로 인한 플래토가 나타나고, 이후 내인성 노화를 반영하는 Gompertz 지수 증가가 뒤따른다. (B) 역사적 사망률 곡선은 시간에 따른 외인성 사망률 감소를 보여준다. (C-D) 유전 그룹 개념도: 외인성 사망률 없을 때 집단 간 분산이 크고 상관관계가 높지만, 외인성 사망률을 추가하면 집단 간 분산이 압축되고 분포가 늘어나 상관관계가 낮아진다. (E-F) Gompertz-Makeham 시뮬레이션: 외인성 사망률 없이 r = 0.37이지만, 역사적 수준의 외인성 사망률($m_{ex}$ = 0.003 year⁻¹) 추가 시 r = 0.13으로 급감한다.
Fig. 1. 외인성 사망률이 쌍둥이 코호트의 수명 상관관계를 은폐한다. (A) 1880년 출생 덴마크 여성의 연령별 사망률: 20~40세 구간에 외인성 사망률로 인한 플래토가 나타나고, 이후 내인성 노화를 반영하는 Gompertz 지수 증가가 뒤따른다. (B) 역사적 사망률 곡선은 시간에 따른 외인성 사망률 감소를 보여준다. (C-D) 유전 그룹 개념도: 외인성 사망률 없을 때 집단 간 분산이 크고 상관관계가 높지만, 외인성 사망률을 추가하면 집단 간 분산이 압축되고 분포가 늘어나 상관관계가 낮아진다. (E-F) Gompertz-Makeham 시뮬레이션: 외인성 사망률 없이 r = 0.37이지만, 역사적 수준의 외인성 사망률($m_{ex}$ = 0.003 year⁻¹) 추가 시 r = 0.13으로 급감한다.
외인성 사망률은 두 가지 경로로 유전율을 낮춘다:
- 유전 그룹 간 분산 $\text{Var}(\mu)$ 감소
- 그룹 내 분산 $\langle\sigma^2\rangle$ 증가 (조기 사망 꼬리 확대)
2. 외인성 사망률 보정 시 유전율 ~50%로 상승
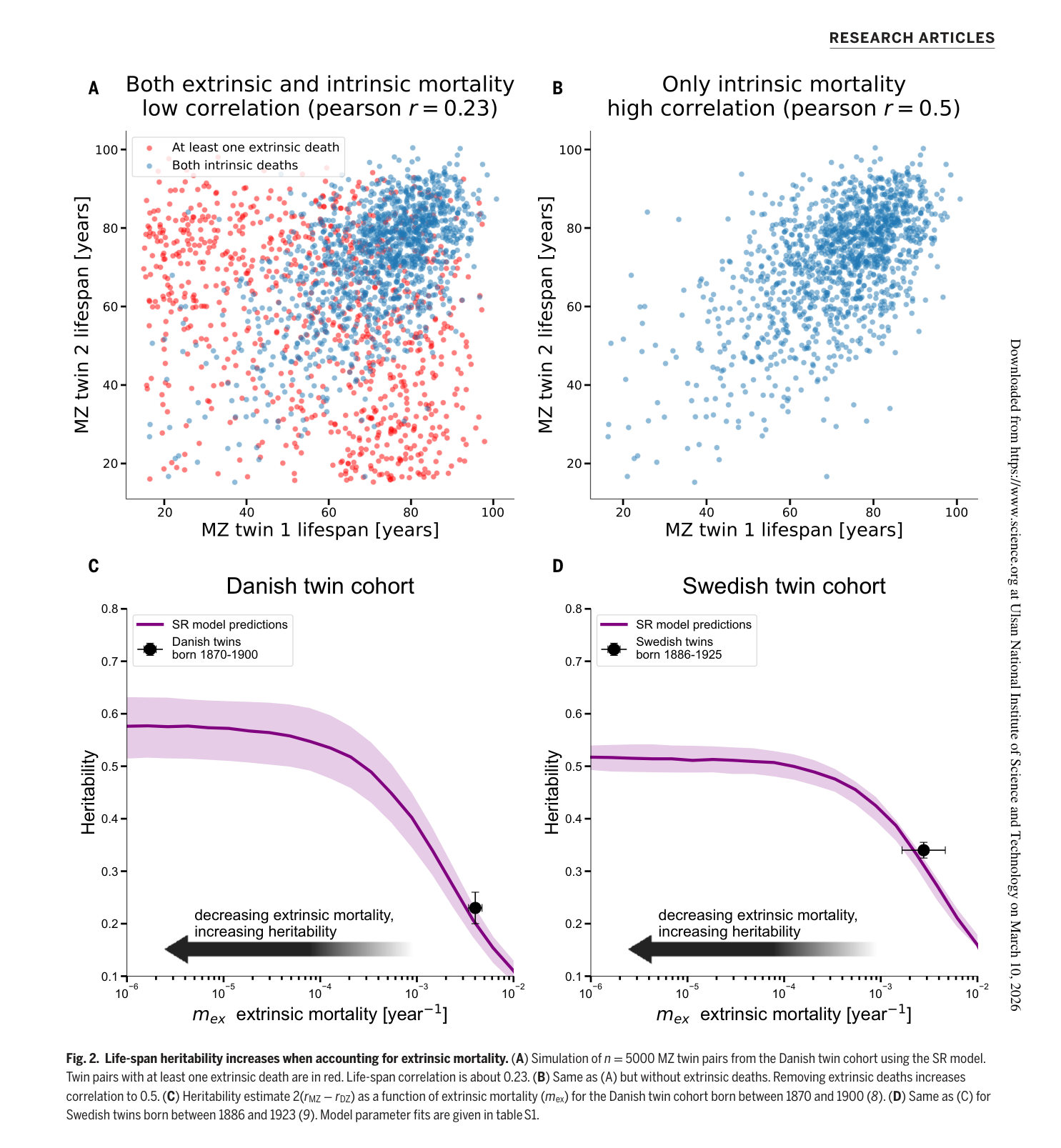 Fig. 2. 외인성 사망률 보정 시 수명 유전율이 증가한다. (A) SR 모델로 시뮬레이션한 덴마크 쌍둥이 코호트 5,000쌍: 빨간 점은 외인성 사망을 포함한 쌍, 피어슨 상관관계 r ≈ 0.23. (B) 외인성 사망 제거 후 상관관계 r ≈ 0.5로 증가. (C) 덴마크 쌍둥이(1870-1900)에서 외인성 사망률($m_{ex}$) 감소에 따른 유전율 $2(r_{MZ}-r_{DZ})$ 변화. (D) 스웨덴 쌍둥이(1886-1923)에 대한 동일 분석. 두 코호트 모두 $m_{ex} \to 0$으로 갈수록 유전율이 약 50%에 수렴한다.
Fig. 2. 외인성 사망률 보정 시 수명 유전율이 증가한다. (A) SR 모델로 시뮬레이션한 덴마크 쌍둥이 코호트 5,000쌍: 빨간 점은 외인성 사망을 포함한 쌍, 피어슨 상관관계 r ≈ 0.23. (B) 외인성 사망 제거 후 상관관계 r ≈ 0.5로 증가. (C) 덴마크 쌍둥이(1870-1900)에서 외인성 사망률($m_{ex}$) 감소에 따른 유전율 $2(r_{MZ}-r_{DZ})$ 변화. (D) 스웨덴 쌍둥이(1886-1923)에 대한 동일 분석. 두 코호트 모두 $m_{ex} \to 0$으로 갈수록 유전율이 약 50%에 수렴한다.
덴마크와 스웨덴 쌍둥이 코호트 모두에서, 외인성 사망률($m_{ex}$)을 0으로 감소시키면 유전율은 점진적으로 증가하여 ~50% 수준에 수렴했다. 이는 역사적 쌍둥이 연구에서 관측된 상관관계의 약 2배에 해당한다.
3. SATSA 연구와 미국 코호트에서의 검증
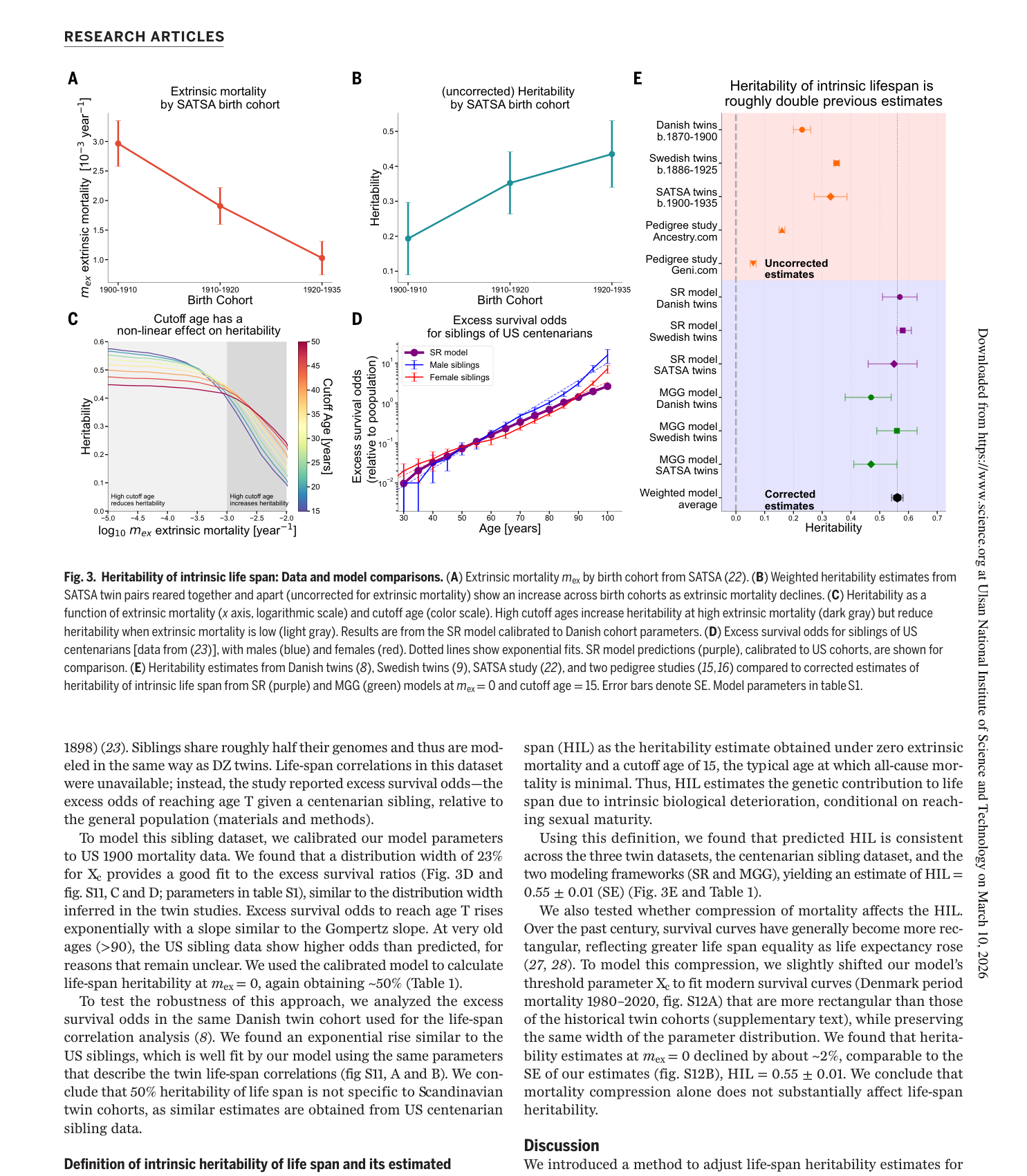 Fig. 3. 내인성 수명 유전율: 데이터와 모델 비교. (A) SATSA 출생 코호트별 외인성 사망률 감소 추세. (B) 외인성 사망률 감소에 따른 SATSA 유전율 추정치 증가. (C) 외인성 사망률(x축 로그 스케일)과 컷오프 연령(색상 스케일)의 함수로서의 유전율: 외인성 사망률이 높을 때는 높은 컷오프 연령이 유전율을 높이지만, 낮을 때는 반대 효과. (D) 미국 백세인 형제자매의 초과 생존 확률 데이터와 SR 모델 예측치. (E) 덴마크, 스웨덴, SATSA 쌍둥이 연구 및 두 족보 연구의 미보정 추정치 vs 보정된 내인성 수명 유전율 추정치 비교 — 보정 후 추정치가 기존 추정치의 약 2배임을 확인.
Fig. 3. 내인성 수명 유전율: 데이터와 모델 비교. (A) SATSA 출생 코호트별 외인성 사망률 감소 추세. (B) 외인성 사망률 감소에 따른 SATSA 유전율 추정치 증가. (C) 외인성 사망률(x축 로그 스케일)과 컷오프 연령(색상 스케일)의 함수로서의 유전율: 외인성 사망률이 높을 때는 높은 컷오프 연령이 유전율을 높이지만, 낮을 때는 반대 효과. (D) 미국 백세인 형제자매의 초과 생존 확률 데이터와 SR 모델 예측치. (E) 덴마크, 스웨덴, SATSA 쌍둥이 연구 및 두 족보 연구의 미보정 추정치 vs 보정된 내인성 수명 유전율 추정치 비교 — 보정 후 추정치가 기존 추정치의 약 2배임을 확인.
SATSA 연구에서는 1900~1935년 출생 코호트를 세 시기로 구분했을 때, 외인성 사망률이 3배 감소하는 동안 보정되지 않은 유전율이 약 2배 상승하는 패턴을 확인했다. 별거 쌍둥이(reared apart)와 동거 쌍둥이(reared together) 추정치가 1 SE 이내로 일치하여 쌍둥이 연구 가정의 타당성을 지지했다.
미국 백세인의 형제자매 데이터도 외인성 사망률 보정 후 유사하게 ~50% 유전율을 나타내, 스칸디나비아 코호트에 국한되지 않는 일반화 가능성을 보였다.
4. 내인성 수명 유전율(HIL) = 0.55 ± 0.01
연구진은 HIL(Heritability of Intrinsic Life span)을 새로운 표준 지표로 제안했다:
- 정의: 외인성 사망률 = 0, 컷오프 연령 = 15세 조건에서의 유전율 추정치
- 의미: 성적 성숙에 도달한 후 내인성 생물학적 퇴화에 의한 유전적 기여도
세 쌍둥이 코호트, 백세인 형제자매 데이터, SR/MGG 두 모델 모두에서 일관되게 HIL = 0.55 ± 0.01 (SE)로 산출됐다.
사망 원인별 유전율 (SATSA 보조 분석)
SATSA 코호트는 암, 심혈관 질환(CVD), 치매 사망 원인 데이터를 포함하고 있어 원인별 분석이 가능했다:
| 사망 원인 | 특징 |
|---|---|
| 암 | 연령 독립적으로 약 0.3의 안정적 유전율 |
| 심혈관 질환 | 80세경 약 0.5, 100세까지 점차 감소 |
| 치매 | 80세경 최고 약 0.7, 이후 0.4~0.5로 안정 |
의의 및 시사점
왜 기존 연구는 유전율을 과소추정했나?
- 역사적 코호트의 높은 외인성 사망률: 18~19세기에는 외인성 사망률이 현재보다 ~10배 높았음
- 사망 원인 데이터 부재: 역사적 쌍둥이 코호트에는 원인별 사망 정보가 없어 보정 불가
- 부적절한 컷오프 연령: 연구마다 다른 최소 포함 연령 사용
- 대규모 족보 연구의 한계: ~300년에 걸친 자기 보고 데이터, 높은 환경적 이질성, 복잡한 동류 교배(assortative mating) 패턴
보정 후 수치가 갖는 의미
55%의 수명 유전율은:
- 마우스 수명 유전율(38~55%)과 유사
- 대부분 인간 생리 형질의 평균 유전율(약 49%)과 일치
- 유전 연구를 통한 노화 메커니즘 이해 가능성을 시사
나머지 ~45%의 분산은?
보정 후에도 수명 변이의 절반 가량은 부가적 유전으로 설명되지 않는다. 이는 다음에서 기인할 것으로 보인다:
- 환경적 영향 (생활 습관, 사회경제적 요인, 의료 접근성)
- 내인성 생물학적 확률성(stochasticity)
- 비부가적 유전 효과 및 후성유전학적 변형
한계점
- 쌍둥이 연구의 기본 가정(“동등한 환경” 가정) 의존
- 보정 방법이 SR 및 MGG 모델 구조에 의존
- 역사적 코호트의 상세한 사망 원인 데이터 부재 — 이를 확보하면 결론에 대한 중요한 검증이 될 것
개인 소감
이 논문의 가장 큰 기여는 측정 방법론 자체를 재검토했다는 점이다. 수십 년간 낮은 수명 유전율이 보고되면서 노화 유전학 연구에 대한 회의론이 커졌는데, 이 연구는 그 원인이 생물학적 사실이 아니라 측정의 교란이었음을 수학적으로 보여줬다.
특히 인상적인 것은 외인성 사망률이라는 단일 교란 요인이 유전율 추정치를 절반 이상 낮출 수 있다는 직관적이지 않은 결과다. MZ 쌍둥이 간 상관관계 공식 $r_{MZ} = \text{Var}(\mu)/(\text{Var}(\mu) + \langle\sigma^2\rangle)$를 생각하면, 외인성 사망률이 분자(집단 간 분산)를 줄이고 분모(집단 내 분산)를 늘리는 이중 효과를 만든다는 설명이 우아하다.
SATSA 코호트를 통한 실증적 검증도 설득력 있다 — 출생 코호트가 달라지면서 실제로 외인성 사망률이 떨어지고, 보정되지 않은 유전율도 예측대로 상승했다. 모델이 데이터를 잘 포착하고 있다는 증거다.
다만 한 가지 주의할 점은, “유전율 55%”가 개인의 수명이 절반 이상 유전자에 의해 결정된다는 의미가 아니라는 것이다. 유전율은 특정 집단, 특정 환경, 특정 시점에서의 표현형 분산 중 유전적 분산의 비율이다. 이 연구가 말하는 것은, 과거보다 균일해진 현대 환경에서 수명 차이를 설명하는 데 유전자의 역할이 기존 추정보다 훨씬 크다는 것이다. 이는 장수 유전자 발굴과 노화 연구에 새로운 활력을 불어넣을 결과다.
References
- Shenhar B et al., Science 391, 6784 (2026)
- Herskind AM et al., Hum. Genet. 97, 319–323 (1996)
- Ljungquist B et al., J. Gerontol. A 53, M441–M446 (1998)
- Kaplanis J et al., Science 360, 171–175 (2018)
- Ruby JG et al., Genetics 210, 1109–1124 (2018)
- Polderman TJC et al., Nat. Genet. 47, 702–709 (2015)
- Klebanov S et al., Genetica 110, 209–218 (2000)
- Pedersen NL, SATSA Study (2005)
- Perls TT et al., Proc. Natl. Acad. Sci. 99, 8442–8447 (2002)
💬 댓글