Lifelong behavioral screen reveals an architecture of vertebrate aging Claire N. Bedbrook†, Ravi D. Nath†, Libby Zhang, Scott W. Linderman, Anne Brunet‡*, Karl Deisseroth‡* Science 391, eaea9795 (2026). DOI: 10.1126/science.aea9795
연구 배경
나이가 들수록 암, 심혈관 질환, 치매 등 만성 질환의 위험이 급격히 증가한다. 고령화 사회가 확대됨에 따라 노화 과정 자체를 이해하는 것이 점점 더 중요해지고 있다. 그러나 노화는 수년에서 수십 년에 걸쳐 일어나는 느린 과정이기 때문에, 개체 단위에서 전 생애를 연속적으로 관찰하는 것은 기술적으로 매우 어려운 일이었다.
발생학에서 배아를 지속적으로 관찰함으로써 발달 과정의 핵심 원리를 밝혀낸 것처럼, 성체 이후부터 노화 사망까지의 전 과정을 연속 추적한다면 완전히 새로운 통찰을 얻을 수 있지 않을까? 이것이 이 연구의 출발점이다.
왜 킬리피시인가?
연구팀은 아프리카 터쿼이즈 킬리피시(African turquoise killifish, Nothobranchis furzeri)를 모델 생물로 선택했다. 킬리피시는 척추동물 중 자연 수명이 가장 짧아(중앙값 4~8개월) 전 생애 연속 추적이 현실적으로 가능하면서도, 텔로미어 단축, 줄기세포 고갈, 면역 노화 등 포유류와 유사한 노화 표현형을 보이는 모델이다.
행동(behavior)은 감각, 인지, 운동 등 다중 장기 시스템의 생리학을 통합하는 풍부한 산출물이다. 연구팀은 이 비침습적 행동 데이터를 통해 노화의 동적 과정을 들여다보고자 했다.
방법론: 전 생애 연속 행동 추적 시스템
 Fig 1. 청소년기부터 죽음까지 연속 행동 추적 시스템의 구성과 데이터 처리 파이프라인
Fig 1. 청소년기부터 죽음까지 연속 행동 추적 시스템의 구성과 데이터 처리 파이프라인
하드웨어 설계
- 개별 수조(2.8L)에 수컷 킬리피시를 개별 수용
- 순환 급수 시스템과 커스텀 자동 급이기(하루 7회, 고정 시간)
- 적외선 카메라로 초당 20프레임 연속 촬영
- 사춘기(성적 성숙, 3~4주)부터 자연사까지 전 기간 기록
데이터 처리 파이프라인
- 키포인트 추출: 딥 CNN으로 매 프레임 6개 신체 키포인트(주둥이, 중체, 후체, 꼬리, 부채꼬리, 옆몸) 예측
- 포즈 특성(Pose features): 속도, 체곡률, 수영 방향 등 57개 특성 계산
- 차원 축소: PCA로 57 → 15개 주성분 (분산 80% 이상 설명)
- 행동 음절(Behavioral syllables): Gaussian HMM으로 100개의 정형화된 서브초 행동 단위 추출
총 3 × 10⁸ 프레임 이상의 데이터를 처리하기 위해 분산 확률적 EM(Expectation-Maximization) 알고리즘을 개발했다. 이를 통해 밀리초(개별 프레임) 단위부터 전 생애(~250일)까지의 다차원 행동 동역학을 체계적으로 분석할 수 있었다.
핵심 결과
1. 전 생애 행동 변화와 개별 노화 궤적
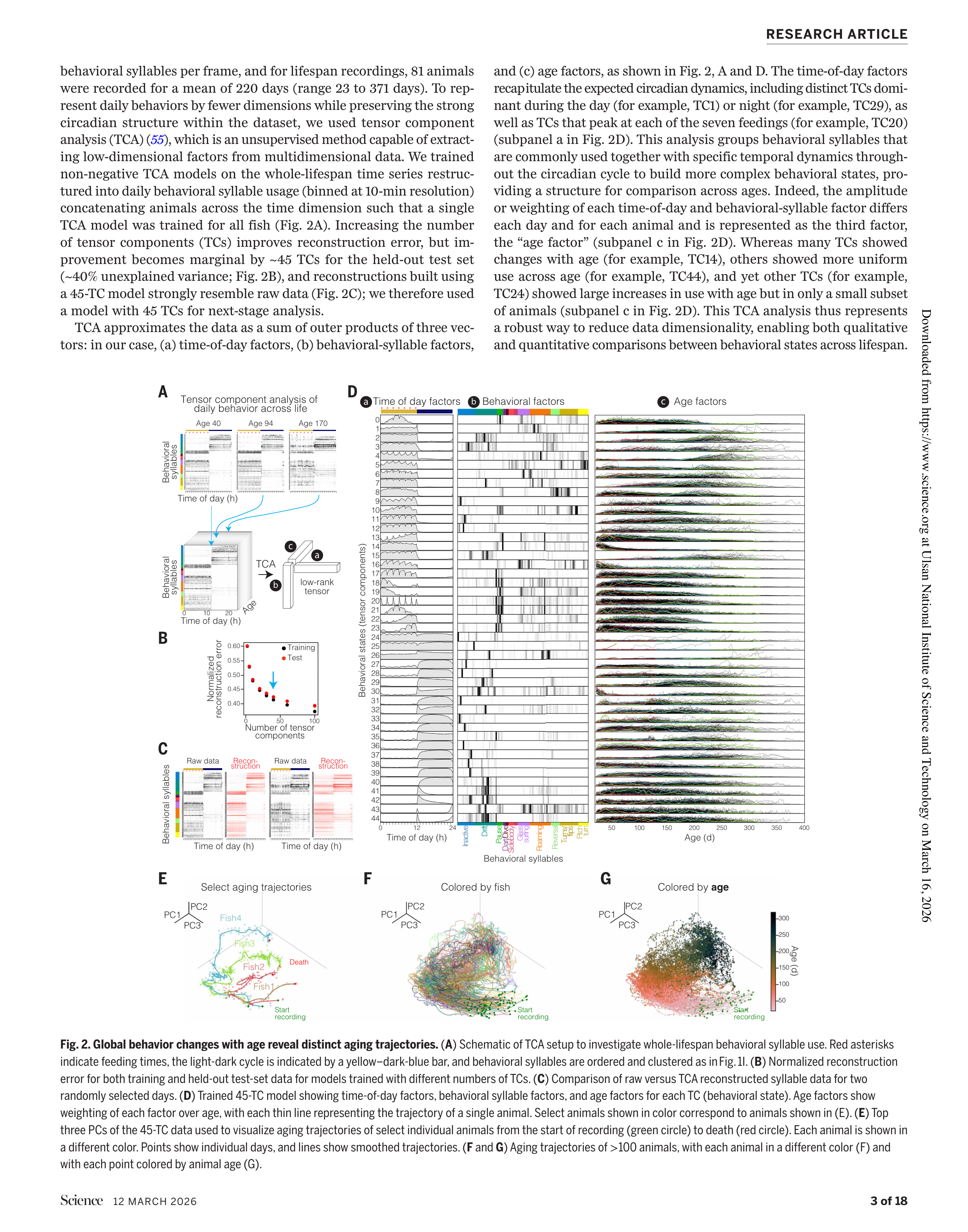 Fig 2. Tensor Component Analysis(TCA)를 통한 전 생애 행동 변화 분석과 개별 노화 궤적
Fig 2. Tensor Component Analysis(TCA)를 통한 전 생애 행동 변화 분석과 개별 노화 궤적
일일 행동 데이터의 고차원성을 해결하기 위해 텐서 성분 분석(TCA)을 적용했다. TCA는 비지도 학습 방법으로, 다차원 데이터에서 저차원 요인을 추출한다. 연구팀은 세 가지 축의 요인을 분리했다:
| 요인 | 설명 |
|---|---|
| 시간대 요인 (Time-of-day) | 일주기 리듬 반영 (주간/야간/식사시간 패턴) |
| 행동 음절 요인 (Behavioral syllable) | 함께 사용되는 행동 패턴의 묶음 |
| 연령 요인 (Age) | 각 TC의 가중치가 나이에 따라 어떻게 변하는지 |
45개의 텐서 성분(TC)을 사용한 모델로 원본 데이터를 충실히 재구성할 수 있었다. 연령 요인의 상위 3개 PC로 시각화한 결과:
- 어린 개체들은 유사한 행동 공간에서 출발하지만, 나이가 들수록 서로 다른 궤적으로 분기
- 개체마다 고유한 노화 궤적을 보임 — 모든 개체가 같은 방식으로 늙지 않는다
- 궤적 상의 위치는 연령과 강하게 상관
2. 수명에 따른 궤적 분기와 분자적 기반
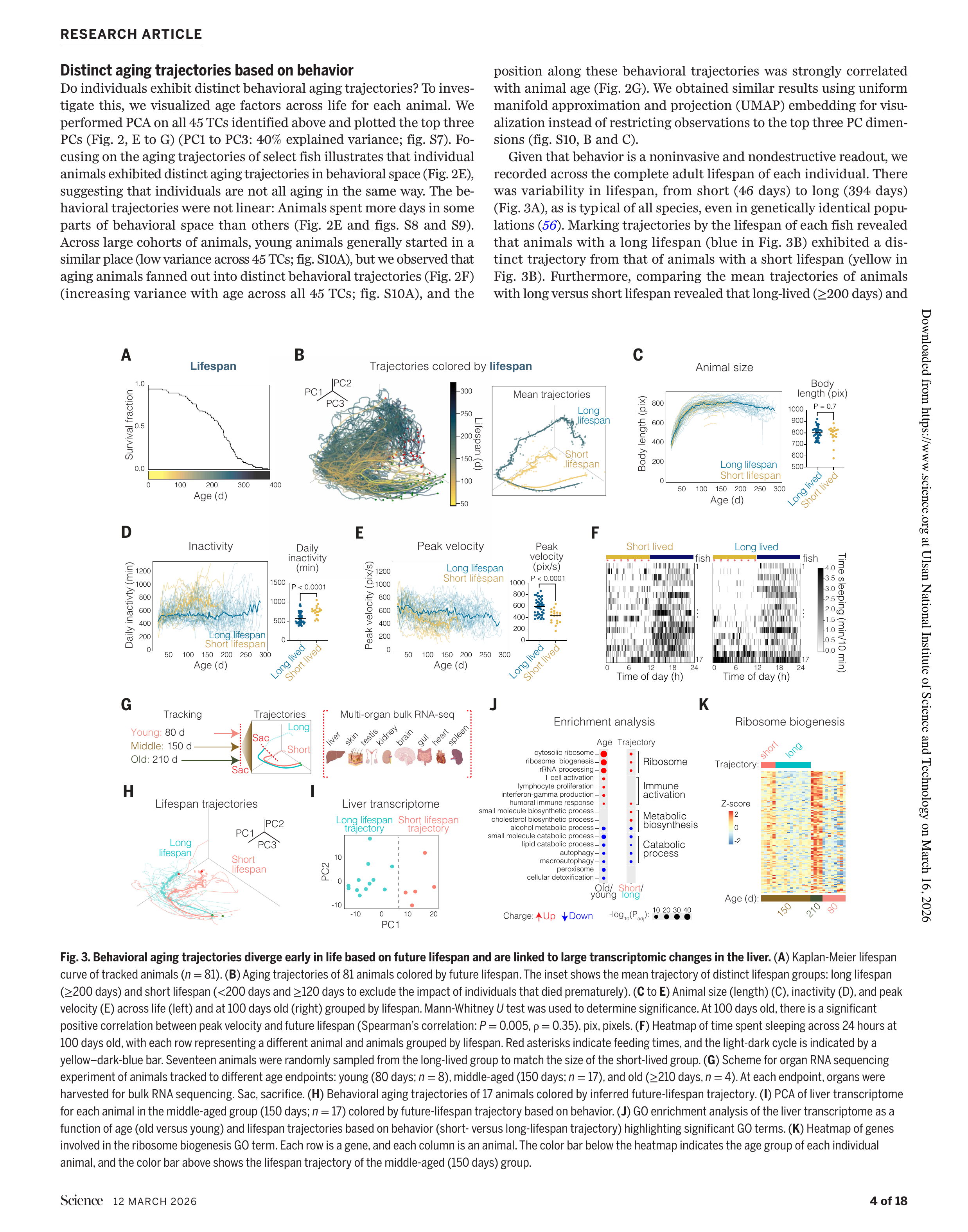 Fig 3. 장수/단명 개체의 행동 궤적 차이와 간 전사체 분석
Fig 3. 장수/단명 개체의 행동 궤적 차이와 간 전사체 분석
장수 개체(≥200일)와 단명 개체(120~200일)는 약 70일경에 궤적이 분기하기 시작했다 — 이는 단명 개체의 사망보다 50~130일이나 앞선 시점이다.
장수 vs 단명 개체의 차이 (100일 시점)
| 지표 | 장수 개체 | 단명 개체 | P값 |
|---|---|---|---|
| 체크기(길이) | 유사 | 유사 | 0.7 |
| 활동 시간 | 유의하게 높음 | 낮음 | < 0.0001 |
| 최대 속도(sprinting) | 유의하게 높음 | 낮음 | < 0.0001 |
| 수면 일주기 패턴 | 야간에 집중 | 주간에도 수면 | — |
흥미롭게도 체크기와 먹이 섭취량에는 차이가 없었다. 장수 개체는 더 활발하고, 더 빠르게 수영하며, 수면 타이밍이 야간에 더 집중되어 있었다.
다중 장기 전사체 분석
연구팀은 행동 궤적으로 장수/단명을 구분한 뒤, 150일 시점에서 8개 장기(뇌, 장, 심장, 신장, 간, 피부, 비장, 고환)의 bulk RNA-seq을 수행했다.
간(liver)에서 가장 뚜렷한 전사체 차이가 관찰되었다:
- 단명 궤적에서 상향 조절: 리보솜 생합성(ribosome biogenesis), rRNA 처리, 번역(translation), DNA 복제
- 단명 궤적에서 하향 조절: 자가포식(autophagy), 이화 과정(catabolic process)
- 노화에서만 변화 (수명 궤적과 무관): 면역 활성화 (T세포 활성화, 림프구 증식, 인터페론-γ)
이 결과는 면역/염증 변화는 노화의 표현형이지 수명을 결정하는 원인이 아닐 수 있음을 시사한다. 반면, 리보솜 생합성의 증가는 단명의 분자적 동인(driver) 후보로 떠올랐다. 이는 리보솜 생합성 감소가 장수 및 장수 개입과 연결된다는 기존 연구들과 일치한다.
3. 행동 기반 연령 시계(Behavioral Clock)
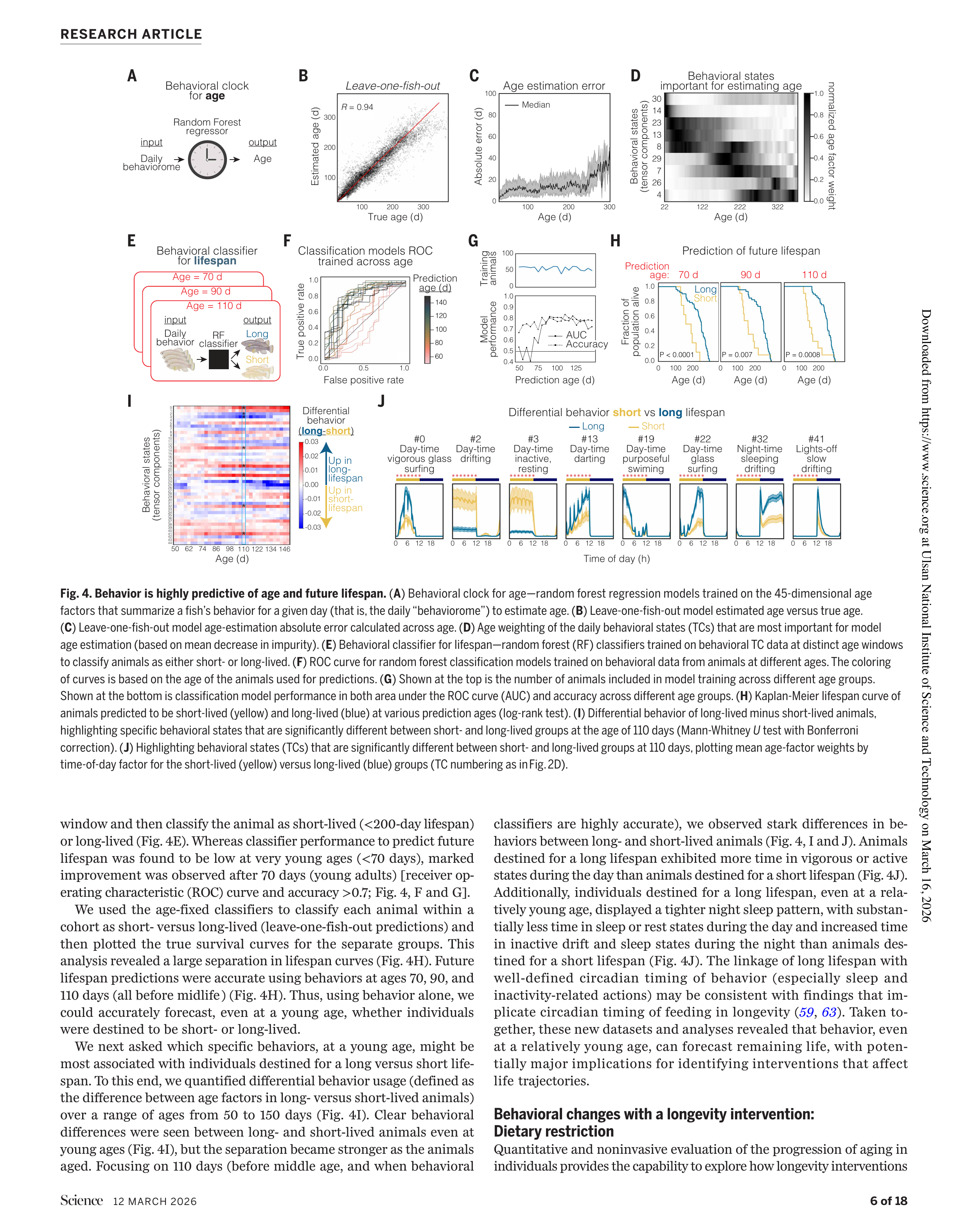 Fig 4. 행동만으로 나이를 추정하고 미래 수명을 예측하는 머신러닝 모델
Fig 4. 행동만으로 나이를 추정하고 미래 수명을 예측하는 머신러닝 모델
연령 추정 (Behavioral Clock)
45차원 연령 요인(일일 행동체, behaviorome)을 입력으로 랜덤 포레스트 회귀 모델을 학습시켜 연령을 추정했다.
- 피어슨 상관계수 R = 0.94
- 중앙 절대 오차(MAE) = 12일
- Leave-one-fish-out 교차 검증으로 평가
연령 추정에 가장 중요한 행동 상태는 나이에 따라 변화했다:
| 연령대 | 핵심 행동 상태 |
|---|---|
| 젊은 시기 | 주간 활발한 수영·탐색 행동 |
| 중년기 | 야간 느린 표류·수면 행동 |
| 노년기 | 일주기 무관한 느린 표류 회전 |
| 초고령기 | 후방 표류·반전 뒤집기 |
이 결과는 노화가 점진적 쇠퇴가 아니라 구별되는 단계들의 연속일 수 있음을 시사한다.
미래 수명 예측 (Lifespan Forecasting)
특정 연령 시점의 행동 데이터만으로 해당 개체가 장수할지 단명할지를 분류하는 모델을 구축했다.
- 70일 이후부터 ROC AUC 및 정확도 > 0.7
- 70일, 90일, 110일 시점 모두에서 정확한 수명 예측 가능 — 모두 중년 이전 시점
장수 예측과 연관된 핵심 행동 특성:
- 주간에 더 활발한 활동 상태
- 야간 수면 패턴이 더 규칙적 (일주기 리듬이 뚜렷)
4. 장수 개입: 식이 제한(Dietary Restriction)의 효과
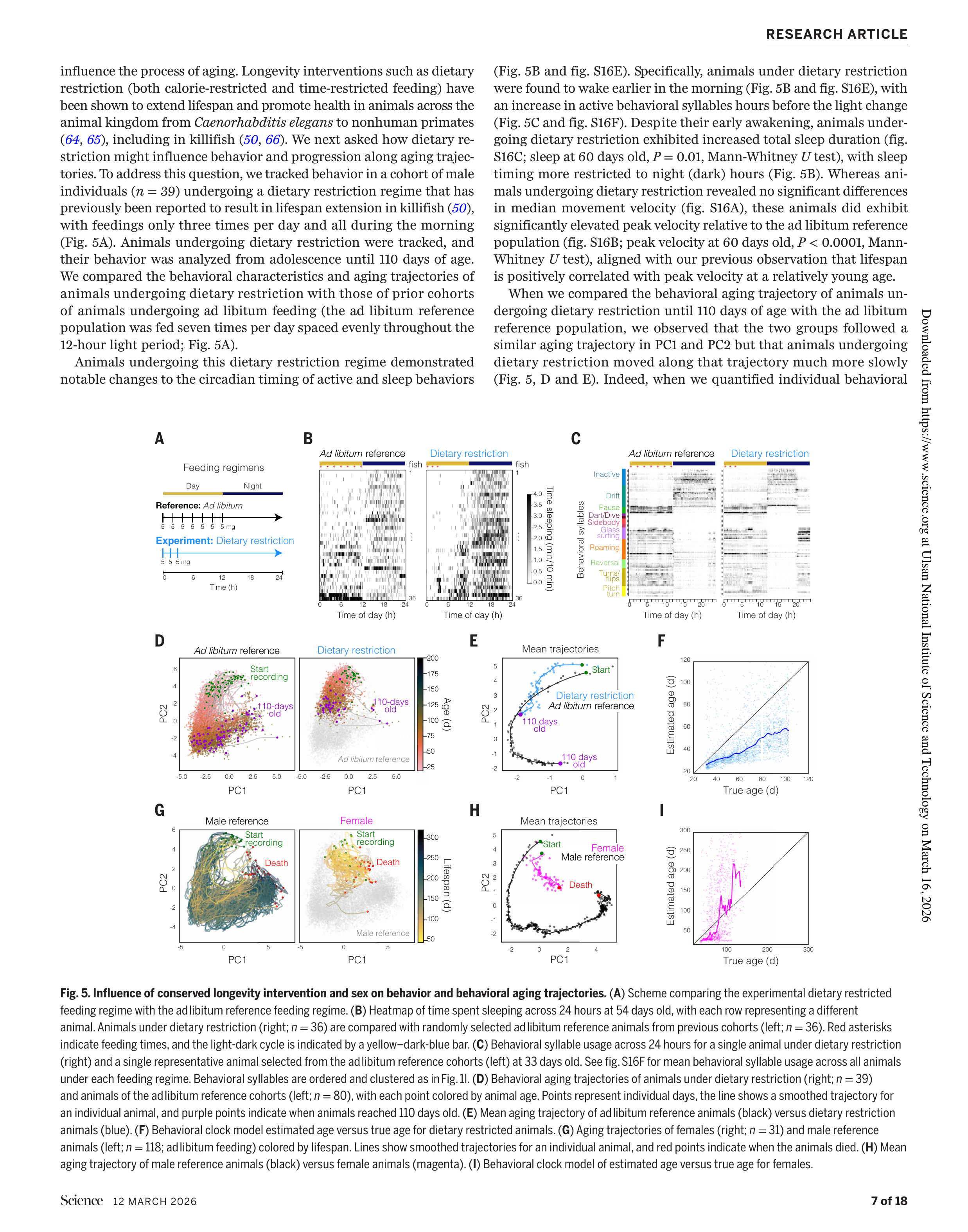 Fig 5. 식이 제한(DR)과 성별에 따른 행동 노화 궤적의 변화
Fig 5. 식이 제한(DR)과 성별에 따른 행동 노화 궤적의 변화
하루 7회 → 3회(오전 집중) 급이로 변경한 식이 제한(DR) 코호트(n=39)를 110일까지 추적했다.
식이 제한의 행동적 효과
- 더 이른 기상: 조명 변화 수 시간 전부터 활동적 행동 증가
- 총 수면 시간 증가: 그러나 수면이 야간에 더 집중 (일주기 리듬 강화)
- 최대 속도 유의하게 증가 (P < 0.0001)
- 행동 노화 궤적의 진행 속도 감소: 같은 방향으로 노화하되, 훨씬 느리게
- 행동 시계 기준 42일 더 젊게 추정됨 (100~110일 시점)
이는 식이 제한이 노화의 경로를 바꾸는 것이 아니라, 동일한 경로를 더 느리게 진행하게 만든다는 것을 의미한다. 칼로리 제한 동물이 대조군과 유사한 질병으로 사망하되 더 늦은 나이에 사망한다는 기존 마우스/영장류 연구와 일치하는 결과다.
암컷의 노화 궤적
암컷(n=31)은 수컷과 완전히 다른 노화 궤적을 보였다:
- 수컷의 단명 개체와 유사한 궤적
- 50일 이전에는 행동 시계 기준 실제보다 젊게 추정되나, 100일 이후 급격히 가속
- 100일 이상 암컷은 실제 나이보다 50~200일 더 늙은 것으로 추정
5. 노화의 구조: 이산적 생애 단계(Life Stages)
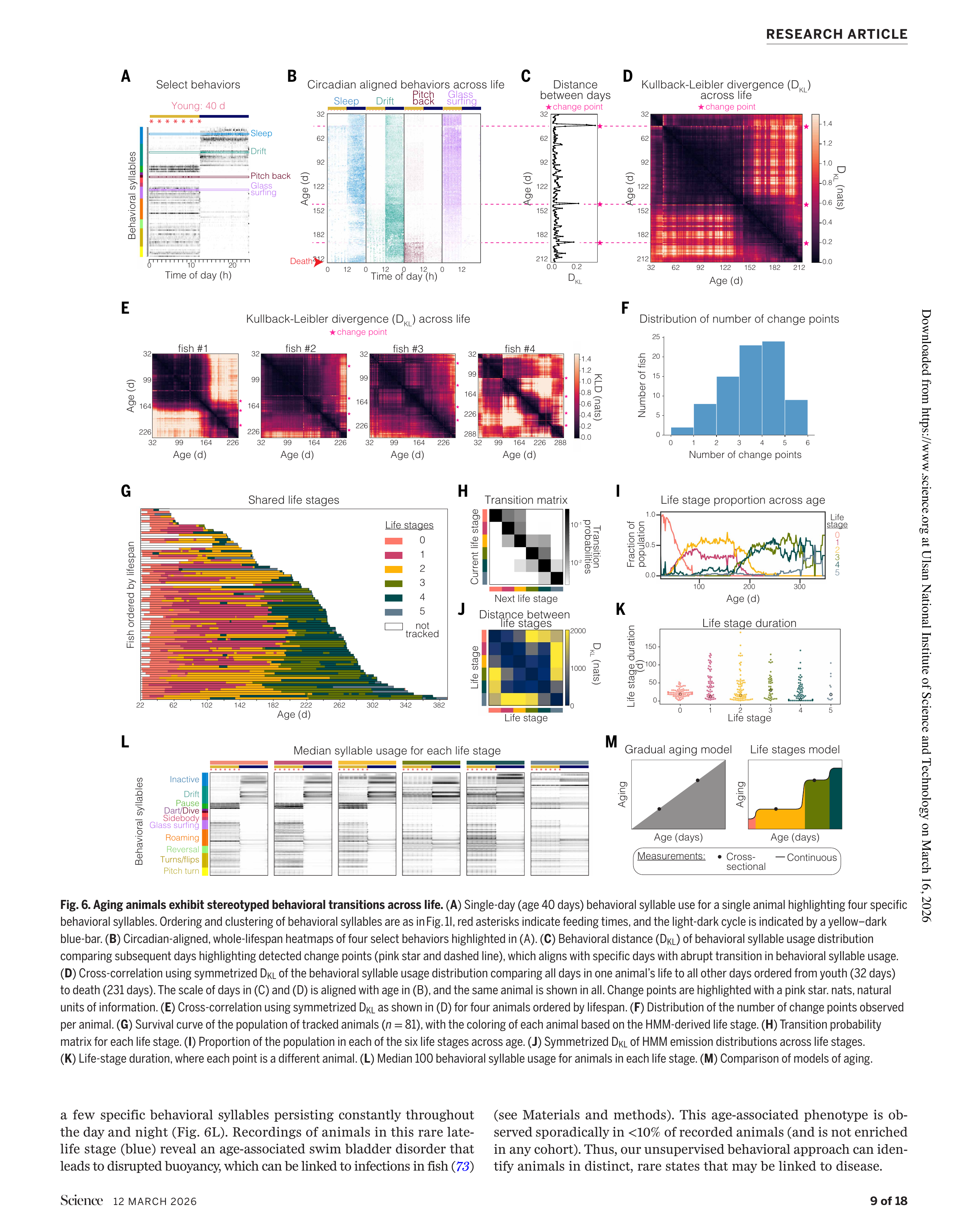 Fig 6. 연속 행동 추적으로 발견한 정형화된 생애 단계 전환
Fig 6. 연속 행동 추적으로 발견한 정형화된 생애 단계 전환
가장 놀라운 발견은 행동이 전 생애에 걸쳐 점진적으로 변하는 것이 아니라, 급격한 전환(abrupt transition)을 동반하는 안정적 단계들의 연속으로 구성된다는 것이다.
변화점 탐지 (Change-point Detection)
- 각 개체의 전 생애 행동을 일별 KL divergence로 비교
- 대부분의 개체에서 3회 이상의 급격한 행동 전환이 관찰됨
- 전환 사이에는 장기간의 안정적 행동 패턴이 유지됨
HMM 기반 생애 단계 모델링
Gaussian HMM으로 6개의 안정적 생애 단계를 식별했다:
| 단계 | 특성 |
|---|---|
| 젊은 단계 (분홍) | 모든 개체가 시작하는 공통 단계 |
| 중년 단계 A (노랑) | 약 절반의 개체가 진입 |
| 중년 단계 B (마젠타) | 나머지 절반의 개체가 진입 |
| 노년 단계 A (연초록) | 일주기 리듬 약화, 주간 수면 증가 |
| 노년 단계 B (진초록) | 행동 유연성 감소 |
| 말기 단계 (파랑) | 부력 장애로 인한 특이 수영 패턴 (<10% 개체) |
핵심적으로, 이 단계들은 순방향으로만 진행하는 특성을 보였다 — 한번 다음 단계로 넘어가면 이전 단계로 되돌아가지 않는다.
노화는 점진적이고 연속적인 쇠퇴가 아니라, 이산적 생애 단계들의 질서정연한 연속이다.
이것이 이 논문이 제시하는 노화의 새로운 구조적 모델이다.
종합 요약
 연구의 전체 개요: 전 생애 행동 스크린을 통한 노화 구조의 발견
연구의 전체 개요: 전 생애 행동 스크린을 통한 노화 구조의 발견
| 발견 | 의의 |
|---|---|
| 개별 노화 궤적의 존재 | 모든 개체가 같은 방식으로 늙지 않음 |
| 행동 기반 연령 시계 (R=0.94) | 비침습적 노화 바이오마커 |
| 젊은 나이에 미래 수명 예측 | 조기 개입 가능성 |
| 리보솜 생합성 ↔ 수명 연관 | 분자적 장수 메커니즘 후보 |
| 식이 제한 → 노화 속도 감소 | 개입의 효과를 행동으로 정량화 |
| 6개 이산적 생애 단계 | 노화 = 단계적 진행, 점진적 쇠퇴 아님 |
개인 소감
이 연구는 “노화를 어떻게 관찰할 것인가”라는 질문에 대한 새로운 답을 제시한다. 3억 프레임 이상의 행동 데이터를 체계적으로 분석하여, 노화가 점진적 쇠퇴가 아니라 질서정연한 단계적 구조를 가진다는 발견은 매우 놀랍다.
특히 인상적인 부분은 세 가지다:
-
젊은 나이의 행동만으로 미래 수명을 예측할 수 있다는 점. 최대 속도(sprinting)와 수면 일주기 패턴이 수명과 강하게 연관된다는 결과는, 인간에서도 보행 속도가 사망률의 예측 인자라는 역학 연구와 맞닿아 있다.
-
면역/염증 변화가 수명 궤적과 무관하다는 발견. 노화와 함께 면역 변화가 일어나지만, 그것이 수명을 결정하는 원인이 아닐 수 있다는 것은 노화 연구의 인과관계 해석에 중요한 시사점이다.
-
식이 제한이 노화 경로를 바꾸는 것이 아니라 속도를 늦춘다는 관찰. 이는 노화 개입의 메커니즘을 이해하는 데 핵심적인 구분이다.
물론 킬리피시에서 발견된 6개 생애 단계가 포유류나 인간에게 직접 적용 가능한지는 추가 연구가 필요하다. 하지만 이 연구가 제공하는 연속적 관찰의 패러다임과 행동 기반 노화 평가의 프레임워크는 향후 노화 연구에 큰 영향을 미칠 것이다.
References
- Bedbrook, C. N., Nath, R. D., Zhang, L., Linderman, S. W., Brunet, A., & Deisseroth, K. (2026). Lifelong behavioral screen reveals an architecture of vertebrate aging. Science, 391(6784), eaea9795.
💬 댓글